
2007年北京市东城区初三下学期综合练习(一)
化学试卷
第I卷(机读卷 共30分)
本试卷分为第I卷(机读卷)和第II卷(非机读卷),满分80分,时间100分钟。
第I卷均为选择题,共30道小题。
可能用到的相对原子质量:、
H―1,C―12,Na―23,O―16,S―32,Cl―35.5,Ba―137,Fe―56
部分碱和盐的溶解性表(

一、选择题(本题包括30个小题,每小题1分,共30分。每小题只有一个选项符合题意)
1.下列都是生活中常见的物质,其中属于纯净物的是( )
A.黄酒 B.冰水 C.碘盐 D.食醋
2.我们每天都和化学变化打交道,以下叙述中没有发生化学变化的是( )
A.吃进的食物一段时间被消化了
B.课外体育活动时,呼吸作用增强
C.水放进冰箱一段时间后结成冰
D.人体吸收氨基酸后,结合成所需的各种蛋白质
3.人类每时每刻都离不开空气,在空气中体积分数约占21%的气体是( )
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
4.用分子的观点对下列常见现象的解释,错误的是( )
A.食物腐败――分子发生变化
B.酒精挥发――分子间间隔变大
C.花香四溢――分子不停地运动
D.热胀冷缩――分子大小随温度变化而改变
5.实验室中装有浓硫酸的试剂瓶应贴有的图标是( )

6.下列图示中物质的用途与相应的性质不相符的是( )

7.某矿泉水标签上印有的主要矿物质成分及含量如下(单位mg/L):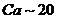 、K~3、Zn~0.06、F~0.02等。这里Ca、K、Zn、F是指( )
、K~3、Zn~0.06、F~0.02等。这里Ca、K、Zn、F是指( )
A.原子 B.离子 C.元素 D.单质
8.生活中常见的下列物质,属于溶液的是( )
A.牛奶 B.泥水 C.蔗糖水 D.花生油
9.有机合成材料的出现是材料发展史上的一次重大突破,下列物质属于合成纤维的是( )
A.棉花 B.羊毛 C.蚕丝 D.尼龙
10.下列实验的基本操作中,错误的是( )
A.用量筒量取液体时,视线与液体凹液面最低处保持水平
B.过滤时,漏斗的下端尖嘴部分紧贴烧杯的内壁
C.测某溶液的pH时,先用水湿润pH试纸,再将被测溶液滴到pH试纸上
D.倾倒液体药品时,试剂瓶上的标签向着手心
11.下列对分子、原子、离子的认识,其中正确的是( )
A.氢原子是最小的粒子,不可再分
B.镁原子的质子数大于镁离子的质子数
C.钠原子易失电子形成带负电的阴离子
D.分子、原子、离子都可以直接构成物质
12.为防止食品变质,常在食品包装盒中放入一小袋用来吸收水分和氧气的物质是( )
A.生石灰 B.固体烧碱 C.碳酸氢钠 D.铁粉
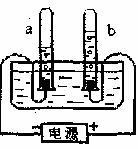
13.根据所学知识,我们可以从“电解水实验”中获得更多的信息和推论。下列说法正确的是( )
A.水是由氢分子和氧分子构成的
B.水是由氢原子和氧原子直接构成的
C.试管a、b中所得气体的体积比约为2:1
D.试管a、b中所得气体的质量比约为2:1
14.根据原子结构示意图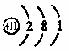 ,不能确定的是( )
,不能确定的是( )
A.无素种类
B.原子的质子数
C.相对原子质量
D.元素的化学性质
15.下列说法错误的是( )
A.实验的操作步骤
粗盐提纯――溶解、过滤、蒸发
点燃气体――先验纯、后点燃
配制溶液――计算、称量、量取、溶解
B.元素与人体健康
人体缺钙――会骨质疏松
人体缺锌――影响人体发育
人体缺铁――易患贫血症
C.生活中的化学知识
海产品保鲜――甲醛水溶液浸泡
油锅着火――立即盖上锅盖
煤炉取暖――放一壶水防CO中毒
D.化学与环境保护
减少水污染――合理使用农药、化肥
减少汽车尾气污染――使用乙醇汽油
减少白色污染――使用可降解的塑料
16.水是人类宝贵的自然资源,下列关于水的叙述中不正确的是( )
A.硬水易生水垢
B.硬水与肥皂作用不易起泡沫
C.可用过滤法分离硬水与软水
D.硬水可以转化为软水
17.施肥是农业增产的重要手段,下列化肥中属于复合肥料的是( )
A.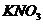 B.
B. C.KCl D.
C.KCl D.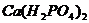
18.下列微粒符号中,对“
A.2Cu中的“
B.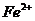 中的“
中的“
C.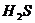 中的“
中的“
D.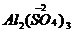 中化学式上方的“
中化学式上方的“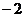 价
价
19.在学习了化学知识后,可以利用家庭生活某些用品进行化学学习和探究活动,下列实验不能利用家庭生活用品完成的是( )
A.验证蛋壳能否溶于酸溶液
B.探究铁制品在什么条件下生锈
C.观察洗涤剂有乳化的功能
D.检验自来水中是否含有氯离子
20.某电池厂排放的污水pH=4,并含有重金属离子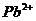 ,合理的治理方案是向污水中加入(
)
,合理的治理方案是向污水中加入(
)
A.生石灰和铁粉
B.石灰石和铜粉
C.纯碱和木炭粉
D.食盐和铝粉
21.科学家通过宇宙探测仪发现金星大气层中含有物质X。X可以通过下列反应制取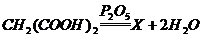 。则物质X的化学式为( )
。则物质X的化学式为( )
A.CO B.CO2 C.C3O2 D.C2O3
22.图表资料可以为我们提供很多信息。下面是某学生对图表资料的理解或使用,其中不正确的是( )
A.根据金属活动性顺序表,判断金属能否置换出稀硫酸中的氢
B.元素周期表是按相对原子质量递增的顺序给元素进行编号的
C.根据溶解度曲线图,判断从溶液中获得晶体的方法
D.根据酸、碱、盐的溶解性表,判断某些复分解反应能否发生
23.“绿色奥运”是2008年北京奥运会的主题之一,为了减轻大气污染,在汽车尾气排放加装“催化净化器”,可将尾气中的NO、CO转化为参与大气循环的无毒的混合气体,该混合气体是( )
A.CO2、NH3 B.O2、CO2
C.N2、CO2 D.NO2、CO2
24.将下列各组物质的溶液混合起来,能发生反应,但无明显现象的是( )
A.NaCl KNO3 B.CuSO4 NaOH
C.AgNO3 HCl D.NaOH H2SO4
25.某溶液中含有大量的氢离子,该溶液一定可以( )
A.跟氯化钡溶液反应
B.跟氧化铜反应得到蓝色溶液
C.跟硝酸银溶液反应
D.用来与块状石灰石反应制取二氧化碳
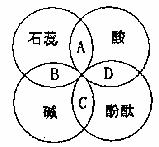
26.小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
27.过氧化氢(H2O2)是一种无色粘稠液体,易分解为水和氧气,常用作氧化剂、漂白剂和消毒剂。为了贮存、运输、使用的方便,工业上将过氧化氢转化为固态的过碳酸钠晶体(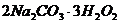 ),该晶体具有碳酸钠和过氧化氢的双重性质。在潮湿空气中接触下列物质不会使过碳酸钠失效的是( )
),该晶体具有碳酸钠和过氧化氢的双重性质。在潮湿空气中接触下列物质不会使过碳酸钠失效的是( )
A.二氧化锰 B.硫酸铜 C.氯化钠 D.盐酸
28.将一定量的镁条投入过量的稀盐酸中,表示反应过程中变化关系的曲线正确的是( )
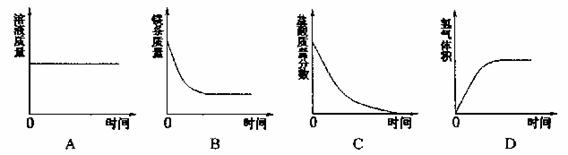
29.把氧化铜和铁粉的混合物加到一定量的盐酸中,搅拌让它们充分反应后,过滤。取滤液加入少量铁粉,无任何现象。则下列判断正确的是( )
A.滤渣中不含铜
B.滤渣可能是铜和铁的混合物
C.滤液中含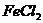 和
和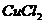
D.滤液中含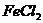 和HCl
和HCl
30.X、Y、W三种物质属于常见的酸、碱、盐,它们在溶液中有如下转化关系:
(1)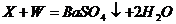
(2)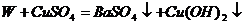
(3)
推断Y的化学式为( )
A.NaHCO3 B.Ba(OH)2
C.H2SO4 D.Na2CO3
第II卷(非机读卷 共50分)
二、填空题(共5个小题,每空1分,共26分。)
31.(5分)自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用下图表示:( 表示氯原子,○表示氧原子,●表示氢原子)
表示氯原子,○表示氧原子,●表示氢原子)

(1)上述物质中,属于单质的有_____________________________(填化学式);
(2)D物质中氯元素的化合价为_____________________________;
(3)D物质中氢、氯、氧元素的质量比(最简整数比)为___________________________;
(4)乙图所示反应的基本反应类型为_____________________________;
(5)以甲图为例,用微粒的观点对质量守恒定律做出解释__________________________
_________________________________________________________________________________________________________________________________________________
32.(5分)认识新能源开发和资源的综合利用具有重要意义。
(1)现在许多地区居民已用上天然气,天然气的主要成分为(写化学式)____________
_____________________________,它与煤和_______________________________________均属于化石燃料。
(2)人们正在利用和开发太阳能、潮汐能及______________________________________(只填一种)等新能源。
(3)现有原煤、铁矿石、焦炭,它们分属于集合A和B,其中A表示自然资源,B表示能源,二者关系如图所示。试将原煤、铁矿石、焦炭填入图中适当的位置。
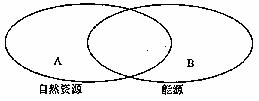
(4)某炼铁厂计划冶炼1000t含杂质3%的生铁,请你帮助计算需要含Fe2O360%的赤铁矿的质量是___________________________________t。
33.(4分)下图甲是A、B、C三种固体物质的溶解度曲线图。
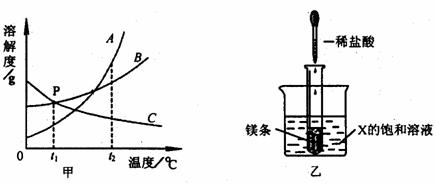
(1)甲图中,t
(2)t℃时,将B物质的接近饱和的溶液转变成饱和溶液可采取的方法有_____________________________(只要求说出两种方法)。
(3)如乙图所示,
34.(5分)一年的化学学习,不但让李丽学到了许多化学原理,更锻炼了她的实验操作能力。她曾为家人和朋友自制果味汽水。她自制各种果味汽水的方法是:在凉开水中加入白糖、果汁、小苏打和柠檬酸。
(1)她加入柠檬酸的目的是_____________________________。
(2)朋友饮用这种汽水时,将瓶盖打开,会有大量气泡冒出,原因是__________________
__________________________________________________________。
(3)她自制的果味汽水中,还缺少人类维持生命和健康所需要的六大营养素中的_____________________________和_____________________________。
(4)在厨房中有食盐和纯碱两种固体,通过化学的学习她认为可以用________________来进行鉴别。
35.(7分)
对物质进行正确的分类,根据各类物质的性质寻找它们之间的反应关系,是学习化学知识的重要方法。
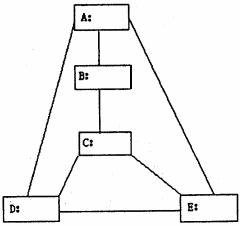
(1)请选择适当的物质填入下图的方框内,使图中直线相连的物质间能发生反应,要求所选物质必须分别属于“金属、非金属、氧化物、酸、碱、盐”六种类别中的四种类别。
(2)根据你所填写的物质,请写出其中D与E之间发生反应的化学方程式___________;该反应属于__________________________________________________________反应(填写基本反应类型)
三、实验题(共3个小题,每空1分,共18分。)
36.(7分)化学上可以通过多种反应得到氨气[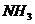 ],(氨气极易溶于水,相同条件下密度比空气小),例如:
],(氨气极易溶于水,相同条件下密度比空气小),例如:
①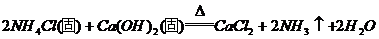
②
③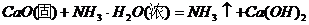
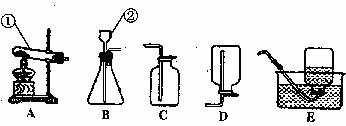
(1)写出标有序号的仪器名称:
①________________________________________
②________________________________________
(2)我将选择反应________________________________________(只写一个,填序号)作为实验室制取NH3的反应原理,我需要用上述装置中的_____________________________(填序号)来制备,用________________________________________(填序号)收集NH3。我选择的发生装置还可用来制________________________________________气体,其反应的化学方程式是________________________________________。
(3)归纳与演绎是重要的科学方法,也是常用的学习方法。我们已经学过实验室制取气体的反应原理、制取与收集方法。请你归纳出实验室制取气体反应的共同点:________________________________________(填序号)。
①需要加热
②使用催化剂
③没有气体参加反应
④原料为纯净物
⑤只生成一种气体
37.(5分)下图是一氧化碳与氧化铁反应的装置图,根据图示回答有关问题:

(1)写出一氧化碳与氧化铁反应的化学方程式__________________________________;
(2)根据此实验可知一氧化碳与二氧化碳的化学性质是不同的,请根据你的认识写出两点:
①________________________________________
②________________________________________
(3)某小组同学欲检验一氧化碳还原氧化铁生成的固体是铁(不考虑有氧化铁剩余),请你简述他们可能设计的一种化学实验方案(包括实验现象、操作和结论)
实验操作
实验现象
实验结论
一氧化碳还原氧化铁生成的固体是铁
38.(6分)一次化学实验课上,小明同学在滴加FeCl3溶液时,不小心把盛有FeCl3溶液的滴管误放入盛“双氧水”(过氧化氢溶液)的试剂瓶中了,但他发现有大量的气泡产生。小明联想到二氧化锰可以做过氧化氢分解的催化剂,那么FeCl3溶液是否也可以做过氧化氢分解的催化剂呢?于是他和同学们对此问题进行了实验与探究。
(1)[提出问题]FeCl3溶液能否做过氧化氢分解的催化剂
(2)[猜想与假设]FeCl3溶液可以做过氧化氢分解的催化剂
(3)[设计与实验]请你帮助他们填写下表:
实验步骤
实验现象
实验结论
①在试管中加入5mL15%的“双氧水”
②滴入适量的FeCl3溶液
③把带火星木条伸入试管
FeCl3溶液可以催化分解过氧化氢
(4)[讨论与反思]已知FeCl3溶液中含有H2O、Fe3+、Cl-等粒子,小明同学又做了三种猜想:
①能够催化分解过氧化氢的粒子是FeCl3溶液中的H2O
②能够催化分解过氧化氢的粒了是FeCl3溶液中的Fe3+
③能够催化分解过氧化氢的粒子是FeCl3溶液中的Cl-
你认为最不可能的是哪一种猜想?其理由是____________________________________。
小明和同学们又对余下的两种猜想,进行了实验探究,请你帮助他们填写下表:
实验步骤
实验现象
实验结论
①向盛有5mL15%的“双氧水”的试管中加入少量盐酸,然后把带火星木条伸入试管
无明显现象
②向盛有5mL15%的“双氧水”的试管中加入少量________________溶液,然后把带火星木条伸入试管
四、计算题(共6分,计算结果除不尽时请保留一位小数)
39.(6分)实验室老师买来一瓶浓硫酸,仔细观察标签,其内容如下图所示:
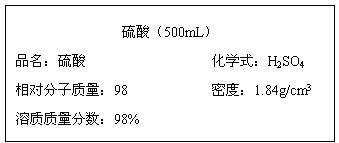
(1)该试剂瓶中硫酸溶液的质量是_______________g,现要将
(2)现有NaCl和BaCl2组成的固体混合物
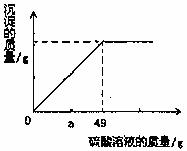
计算固体混合物中 的质量分数是多少?(写出计算过程)
的质量分数是多少?(写出计算过程)
(3)如图所示,若a为24.5时,将所得混合物过滤,除去沉淀,此时滤液中的溶质为_____________________________________(写化学式)。再将所得滤液蒸干,求得到的固体混合物中各成分的质量比为_____________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com