
2006-2007学年度潍坊市诸城九年级下学期
单元过关考试(四)
参考相对原子质量:H--1 O--16 S--32 Na--23 Cl--35.5
一、选择题(本题包括5小题,每小题2分,共10分。每小题只有一个选项符合题意)
1.下列过程中,只涉及物理变化的是
A.维生素C将食品中的三价铁还原
B.用燃烧实验鉴别天然纤维和合成纤维
C.净化水时的吸附、沉淀、过滤和蒸馏操作
D.葡萄糖在酶的作用下转变成二氧化碳和水
2.下列说法中错误的是
A.水分子是保持水的化学性质的最小粒子
B.原子在化学变化中不能再分
C.离子一定是带电的粒子
D.CO(NH2)2中氧元素与氮元素的个数比为1:2
3.室温时,不饱和的食盐水在空气中露置一段时间后,有少量晶体析出,对于该溶液,下 列说法正确的是
A.溶质的溶解度减小 B.溶质的质量不变
C.溶质的质量分数减小 D.溶液变成饱和溶液
4.生产生活中常用到下列物质,其中属于纯净物的是
A.蒸馏水 B.氨水 C.不锈钢 D.碘酒
5.鉴别一瓶水是蒸馏水还是山泉水的最可靠的方法是
A.看是否澄清 B.用肥皂水鉴别
C.品尝味道 D.嗅闻气味
二、选择题(本题包括12小题,每小题3分,共36分,每小题只有一个选项符合题意)
6.下列做法中,能减缓化学反应速率的是
A.面团发酵时放在温热处
B.人在进食时细细咀嚼食物
C.在食品密封包装时充入氮气
D.煤燃烧时向煤炉中鼓入空气
7.对于化学反应A+B=C+D的下列说法中正确的是
A.若生成物C和D分别是盐和水,则该反应一定是中和反应
B.若A和C是单质,B和D是化合物,则该反应一定是置换反应
C.若A是可溶性碱,B是可溶性盐,则C和D不可能是两种沉淀
D.若A、B、C、D都是化合物,则该反应一定是复分解反应
8.实验前恰当处理实验用品是保证实验成功的关键,下列处理方法中,错误的是
A.配置一定质量分数的氯化钠溶液,所用烧杯需要干燥
B.用pH试纸测定溶液的酸碱度,需先将试纸用水湿润
C.做铝条与硫酸铜反应实验,铝条需要用砂纸打磨
D.进行过滤操作,需先将滤纸润湿使之紧贴漏斗内壁
9.钛和钛的合金被认为是21世纪的重要材料,它们具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工,钛合金与人体有很好的“相容性”等。根据它们的主要性能,下列用途不切合实际的是
A.用来做保险丝 B.用于制造航天飞机
C.用来制造人造骨 D.用于制造船舶
10.用稀盐酸和酚酞混合液在白纸上画图,晾干后加入下列物质能使此纸上出现红色图像的是
A.过量盐酸 B.水中溶有三氧化硫的溶液
C.过量氢氧化钠溶液 D.适量石蕊试液
11.硝酸铁溶液中混有少量硝酸银和硝酸钡杂质,用下列哪种方法除杂质可得到纯净的硝酸铁溶液
A.先加适当盐酸,再滴加适量硫酸
B.先加入适量氯化钡,再滴入适量硫酸铁溶液
C.加入适量碳酸钠
D.先加入适量氢氧化钠,再滴入适量氯化钾溶液
12.杂志评出2004年十大科技突破,其中“火星上‘找’到水的影子”名列第一,这一科技突破与下列关于水的说法联系最密切的是
A.生命的孕育和维系需要水 B.水的固体、液体、气体三种状态
C.水电解时生成氢气和氧气 D.水是化合物
13.同学们在做实验时发现,将镁条放入某CuCl2溶液中,镁条表面有气泡产生,对于这一异常现象产生的原因,同学们设计了以下探究方案进行讨论。其中没有意义的是
A.甲同学推测该气体可能是H2,并收集气体用点燃法检验
B.乙同学猜想该CuCl2溶液显酸性,并用pH试纸检测
C.丙同学用锌粒与该CuCl2溶液反应,观察是否有气泡产生
D.丁同学用镁粉与该CuCl2溶液反应,观察产生气泡的快慢
14.下列厂商的做法没有损害消费者权益的是
A.食品厂用CuSO4溶液浸泡粽叶,让已经失去原色的粽叶返青,使粽子表面变得鲜绿。 B.用矿物油对过期的大米进行抛光,使大米看上去色泽鲜亮。
C.用硫黄燃烧熏蒸银耳,使之漂白。
D.在牛奶中加入适量乳酸钙,帮助人们补充钙元素
15.下列叙述中,错误的是
A.铵态氮肥不能与草木灰(主要成分是碳酸钾)混合施用
B.在煤中加入石灰石和生石灰作固硫剂以减少空气污染
C.在图书档案、贵重设备、精密仪器等发生火灾时,可用泡沫灭火器扑灭
D.油污可以被洗涤剂通过乳化作用除去
16.实验室中的试剂常因与空气中的一些成分作用而发生变化,下列对试剂在空气中发 生变化的分析不正确的是
A.铁粉生锈与空气中的水蒸气和氧气有关
B.氢氧化钠潮解变质与空气中的水和二氧化碳有关
C.氧化钙的变质与空气中的水和二氧化碳有关
D.浓盐酸变稀与空气中的水蒸气有关
17.如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是 
A.甲、乙、丙三种物质的溶解度由大到小的顺序是甲>乙>丙
B.t℃时,三种物质的饱和溶液中溶质质量分数由大到小的顺序是甲>乙>丙
C.降低温度可以使丙的不饱和溶液变为饱和溶液
D.将t℃的三种饱和溶液降温至
三、(本题包括5小题,每空1分,共29分)
18.利用化学知识,可以防止生活中一些不利现象的产生。
(1)为保证人身安全,进入久未开启的菜窖前,须做 试验。
(2)为防止照片褪色,可将照片塑封(用塑料薄膜封闭起来)。目的是隔绝
(3)2005年哈尔滨发生严重的水污染事件,有关部门利用大量活性炭使水质净化,这是利用了活性炭的 性
(4)为延长食品保质期,有些食品袋内放有一包“双吸剂”(主要成分是活性炭、铁粉),这里“双吸”所吸收的物质指的是 和 。
19.《中国剪报》最近报道,慢性腹泻患者宜喝酸牛奶。酸牛奶中酪蛋白易于消化吸收,能使胃容物的酸性增强,还可促进钙的吸收
(1)喝酸牛奶后,胃容物的pH (填“增大”或“减小”)
钙尔奇D600一
主要成分:碳酸钙
维生素D
服用方法:咀嚼或水服
贮藏:密封避光
(2)“别把含乳饮料当作牛奶喝”,是因为含乳饮料中 等营养素的含量比牛奶和酸牛奶低。
(3)“钙尔奇D”是一种常见补钙剂,如图是“钙尔奇D”说明书的一部分。思考后,请完成以下任务:写出胃液与“钙尔奇D”反应的化学方程式 反应类型: 。
因此碳酸钙在医疗上还可以用来治疗 症,由贮藏方法分析推断维生素D可能具有的性质是 。
(4)钙尔奇D具有良好的补钙效果,因为本产品中的维生素D的功能是 。维生素D属于六大营养素中的 。
20.将20ml水倒入装有20ml95%的酒精的烧杯中,混合均匀后体积为Vml,再将一块手帕浸入该溶液中,用镊子夹起手帕,点燃手帕上的酒精,当手帕上的火焰即将熄灭时,将手帕晃动几下,火熄灭,手帕完好无损。
(1)混合后的溶液中溶质是 。
(2)混合后的体积VmL 40ml。(填“>”“<”或“一”),原因是
(3)手帕完好无损的原因是
21.北京
(1)造成酸雨污染呈加重趋势的原因是(写一种)
(2)每个家庭都离不开燃料。你家使用的燃料是 ,你家在使用燃料时,使燃料充分燃烧的方法是 如果燃烧不充分可能产生的后果是 。
(3)山西污染指数中居首位的是可吸入颗粒物,这与所处地区自然资源与工业生产直接相关,你认为造成空气中可吸入颗粒物增多的原因是(写一种)
(4)取海河水系某支流河水分析,其主要污染物有较多悬浮物,河水呈碱性,水中含较多 CO32-和有机物质(淀粉、蛋白质、洗涤剂等),还有大量病原体(如细菌、寄生虫等)
①用pH试纸测定河水酸碱度的方法是
②要除去水中的细小颗粒,可在水中加入 (填物质名称)作净水剂,然后静置处理。
③要除去水体中较多的CO32,并使水体呈中性,可加入的物质是(写一种) 。
④为有效消除水体中的病原体,可选用下列物质中的 。
A.二氧化碳 B.漂白粉 C.氧气 D.石子和细沙
22.取两块大小相同的干冰,在干冰中央挖一个小穴,撒入一些镁粉,用红热的铁棒把镁点燃,将另一块干冰盖上,你会看到镁粉在干冰内继续燃烧,发出耀眼的白光,像冰灯一样。已知该反应的生成物是氧化镁和碳。该实验证明干冰具有 的性质(答一条即可);为验证上述反应所得固体中无剩余的镁,可向该固体中加入试剂的名称为 ,反应的现象是
四、(本题包括2小题,第1小题9分,第2小题10分,共19分)
23.硫酸亚铁是一种重要的化工原料,用途十分广泛,如医疗上可用于治疗缺铁性贫血;农业上可施用于缺铁性土壤等。某校化学兴趣小组,利用工业废铁屑为原料设计如下两种制备硫酸亚铁的方案:
①Fe + H2S04==FeS04 + H2↑
②2FeO + 4H2S04(浓)==Fe2(S04)3+S02↑十+4H20 Fe + Fe2(S04)3==3FeS04
(1)两种方案都有一定的理论依据,他们选用了方案①,那么不用方案②的理由是
(2)实验过程中,如何判断方案①的反应已经停止
(3)利用工业废铁屑为原料制备FeSO4的现实意义是:
(4)工业废铁屑常沾有油污,去除油污的方法是
(5)他们在配制所需的稀硫酸时使用了自来水,小明提出自来水中含有少量的Cl-会影响到制出的FeS04的纯度,请你设计实验证明已配制的稀硫酸中混有Cl-
实验步骤
实验现象
结论
24.2003年6月,西安北郊古墓中出土二青铜锤(一种酒具),表面附有绿色固体物质,打开盖子酒香扑鼻,内盛有
(1)如果让你对出土的“西汉美酒”进行探究,你想探究的一个问题是:
(2)上述报道引发了某校初三化学兴趣小组同学的关注,他们收集家中铜器表面的绿色固体,进行探究。

(3)提出问题:铜器表面附着的绿色固体物质是由哪些元素组成的?猜想:查阅相关资料后,猜想绿色固体物质可能是铜绿。
设计与实验:
①对试管内的绿色固体加热,至完全分解。观察到A装置中绿色固体逐渐变成黑色,B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸,观察到黑色固体逐渐溶解,溶液变成蓝色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。观察到铁丝表面有红色物质析出。实验结论:绿色固体物质中含有 、 、 、 等元素。(提示:装置内的空气因素忽略不计)
表达与交流:
①图中标有a.b的仪器名称是:a b
②上述③中发生反应的化学方程式为
③反应完成后,如果先移去酒精灯,可能出现的现象是:
④如果将B、C两装置对调,行吗?为什么?
五、计算题(本题包括1小题,共6分)。
25.
求:(1)需要此NaOH溶液多少克?
(2)反应后所得溶液中溶质的质量分数
附加题(本题包括1小题,共10分,计入总分,但整卷总分不超过100分)
某化学兴趣小组在做Fe和CuS04溶液反应时,发现生成Cu的同时有气泡产生,为了进一步研究做了如下实验:
(1)取8.
(2)将9.
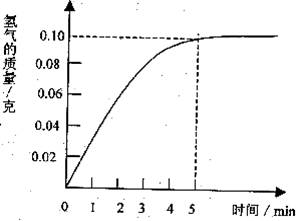
求:(1)稀盐酸的质量分数及与稀盐酸反应的Fe的质量
(2)与CuSO4反应的Fe的质量
(3)与CuSO4反应的Fe的质量及与盐酸反应的Fe的质量之和
8.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com