
2007-2008学年度东营市利津县第一学期期中考试
九年级化学试题
可能用到的相对原子质量:Fe 56 Mg 24 Zn 65 Cu 64 H l S 32 O 16
一、选择题(本题包括l2个小题,每小题3分,共36分。每题只有一个选项符合题意)
1.在社会主义新农村建设中,农民的生活质量和生活条件有明显改善,下列选项中对新农村建设没有促进作用的是( )
A.合理使用农药,减少农药对农产品和环境的污染
B.清洁能源代替化石能源,减少化石燃料燃烧对空气的污染
C.农村中有大量天然的井水,不须消毒杀菌便可直接饮用
D.垃圾进行无害化处理,减少对土壤和地下水的污染
2.下面是小明同学用连线的方式对某一主题知识进行归纳的情况,其中有错误的一组是( )
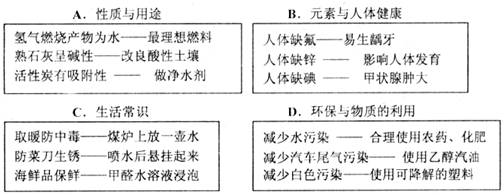
3.下列说法错误的是( )
A.化学反应是人类获取能量的重要方式
B.中Ca2+、Mg2+的增多会引起水体的富营养化
C.煮沸或蒸馏的方法能降低水的硬度
D.铁在潮湿的空气中容易生锈
4.某环保监测站取刚降下的雨水,每隔一定时间测定其pH,数据如下:
测定时间/分钟
0
l
2
4
5
pH
4.73
4.62
4.56
4.55
4.55
下列有关说法不正确的是( )
A.雨水酸性逐渐减弱
B.一段时间后雨水酸性渐趋稳定
C.酸雨可腐蚀某些建筑物和金属制品
D.酸雨是由于空气受硫的氧化物或氮的氧化物污染形成的
5.某新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属线,当玻璃被击碎时,与金属线相连的警报系统就会立刻报警。“防盗玻璃”能报警,这利用了金属的( )
A.延展性 B.导电性 C.弹性 D.导热性
6.下列关于生活常识的说法中,正确的是( )
①小苏打是治疗胃酸过多症的一种药剂
②香烟的过滤嘴可滤除CO等有害物质,故吸烟对身体无害
③摄入过多量重金属盐会使人中毒
④食用霉变食品可使人引发肿瘤等恶性疾病
A.只有①② B.只有①②③ C.只有①③④ D.只有①④
7.“信息”、“材料”和“能源”被称为新科技革命的三大支柱。下列叙述不正确的是( )
A.核能、太阳能、氢能等是具有广阔开发前景的新能源
B.制造“神州五号”宇宙飞船,使用了大量新型材料
C.有机高分子材料的广泛应用“有百利而无一害”
D.人类应与环境和谐相处,要合理开发和利用化石燃料等矿物资源
8.等质量的稀硫酸分别与足量的镁、铁、锌三种金属反应,下列图像能正确生产氢气质量与反应时间之间关系的是( )

9.化学的研究目的就是帮助人们认识、改造和应用物质,把金属矿物冶炼成金属就是人们利用化学方法实现物质改造的典型范例。下表中不同的金属被开发和利用的年代不同,从化学反应的角度看,决定这一年代先后顺序的关键因素是( )
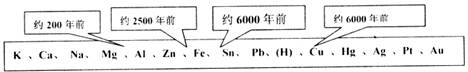
A.金属的活动性 B.金属的导电性
C.金属的延展性 D.地壳中金属元素的含量
10.图表资料可以为我们提供很多信息,下列从图表中获取的信息及应用不正确的是( )
A.根据金属活动性顺序表,判断金属是否容易被盐酸腐蚀
B.根据金属的熔点数据表,判断金属的导电性强弱
C.根据溶解度曲线图,选择从溶液中获得晶体的方法
D.根据元素周期表,查找元素的原子序数、元素符号、相对原子质量
11.某单质X能从某溶液中置换出单质Y,由此推断F列说法中正确的是( )
A.X一定是排在金属活动顺序表中氢以前的金属
B.X是金属时,Y可能是金属,也可能是非金属
C.X是金属时,Y一定比X活泼
D.X、Y都是金属时,Y一定比X活泼
12.金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组在实验室探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度足量稀盐酸中,观察现象如下:
金属
Ti
Mg
Cu
金属表面现象
放出气泡速度缓慢
放出气泡速度快
无变化
下列有关三种金属的说法正确的是( )
A.三种金属的活泼性由强到弱的顺序是:Ti、Mg、Cu
B.若Ti粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D.温度、金属表面积、盐酸浓度等因素都会影响反应速率
二、填空(包括5个小寇,共38分)
13.(8分)从K、C、S、H、O、N六种元素中选择适当的元素按要求填空。
(1)用适当的数字和符号填空:①两个钾离子 ;②一个碳酸根离子 ;③双氧水中氧显一l价 。
(2)写出符合下列要求的物质的化学式:
①能灭火的气体是 ; ②充入食品包装袋中可防腐的单质是 ;
③可作复合肥料的是 ; ④能形成硫酸型酸雨的空气污染物是 ;
⑤溶于水使溶液温度显著降低的是 。
14.(6分)不到一年,你就初中毕业了。设想离开母校之际,你要留下最后一个好印象,做到爱护学校的一草一木,不乱扔东西……假设你在整理自己的东西时,清理出如下物品:A、废作业本,B、烂苹果,C、易拉罐瓶,D、霉变了的饼干,E、生锈的铁钉。
(1)你应放入“可回收垃圾箱”的是 (填序号);
(2)你用盐酸除去铁钉上的铁锈(主要成分是Fe2O3),以重新使用,请写出除锈的化学方程式 。
(3)请你写一句劝告其他年级同学爱护学校环境的话语。
15.(8分)下表为某品牌燕麦片标签中的一部分:
(1)下表表出现了六大类营养素之中的 类。
(2)下表出现了 种人体所需的微量元素。
(3)人体健康离不开钙元素,下列有关钙元素的叙述不正确的是(填序号)
①人体中钙元素大部分存在骨骼和牙齿中
②幼儿及青少年缺钙会得佝偻病和发育不良
③老年人缺钙会发生骨质疏松,容易骨折
④成年人比幼儿和青少年需要摄入更多的钙
(4)假设每克蛋白质完全氧化放出热量约为18KJ,则每
营养成分 每
蛋白质(g) 7.4
糖类(g) 7.8
脂肪(g) 7.9
钙(mg) 206
铁(mg) 19.2
钠(mg) 37.8
锌(mg) 10.1
维生素(mg) 18
16.(8分)物质X和A~F都是初中化学中的常见物质,且有如图所示的转化关系。已知A、D为碱溶液,回答下列问题:

(1)写出下列物质的化学式:X 、E 。
(2)写出下列反应方程式:X+A: ;
D+CuCl2→E+F: 。
17.(8分)陶是人类最早利用化学反应制造的人造材料,青铜是人类最早用化学反应制造的金属材料。陶器、青铜器及铝器的广泛使用,极人地促进了人类社会的发展。请回答下列问题:
(1)陶、铜、铁等材料的生产离不开火,火即所谓的燃烧,其实质是一种(填反应类型) ____反应;而铜和铁的冶炼,主要是利用(填反应类型) 反应把铜和铁从其的化合物中转化出来。
(2)制陶的原料是黏土,其主要成分是二氧化硅、氧化镁、氧化铝和碳酸钙。当温度达到
(3)在生产和生活中,大量使用的不是纯金属,而是它们的合金。合金与纯金属比较,其优越的性能有(答出一条即可) ,原因是 。
三、实验探究(包括2个小题,共20分)
18.(14分)某研究性学习小组设计的实验装置(如下图),既可用于制取气体,又可用于验证物质性质。
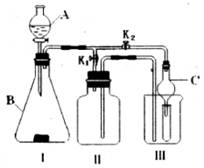
(1)写出仪器A和B的名称:
A ;B 。
(2)当打开K1、关闭K2时,利用Ⅰ、Ⅱ装置可直接进行的实验是 (填序号)。
①大理石与稀盐酸反应制取二氧化碳
②锌与稀硫酸反应制取氢气
小颖认为在不改变Ⅰ、Ⅱ装置的仪器及位置的前提下,该装置可用于双氧水制取氧气,她的做法是 ;实验室还可以用高锰酸钾制取氧气,化学方程式为 。
(3)当打开K2、关闭K1时,利用Ⅰ、Ⅲ装置可验证二氧化碳与水反应,生成了碳酸,此时试管中盛放的物质是 ,可以观察到的现象是 (C为干燥管,用于防止液体倒吸)。
19.(6分)铝是重要的轻金属,广泛应用于航空、电讯和建筑等领域。铝亦有其特殊的性质,试根据以下信息填空或简答。
(1)按金属的活动性顺序,铝比锌 。但是将铝片和锌粒分别投入稀硫酸中,铝片表面产生的气泡却比锌粒少而慢。为了探究铝与酸反应的规律,小强将已被砂纸打磨过的相同大小的6枚铝片,分别放入下表所示溶液中进行实验。
溶液
现象
溶液
现象
溶液
现象
①稀硫酸
一
③稀硫酸(加入少量Na2SO4固体)
一
⑤盐酸
(1:4)
+
②稀硫酸
(加热)
+
④稀硫酸(加入少量NaCl固体)
+
⑥盐酸
(37%)
++
注:“一”表示铝表面产生气泡很小且慢;“+”表示铝表面产生气泡较大且快。“1:4”表示用1体积的37%浓盐酸与4体积的水混合所得溶液。
根据上述表格内容,你认为铝与酸反应产生氢气的速率,除了跟酸溶液中氢离子浓度有关外,还可能受到 、 、 等多种因素的影响。
(2)小芳将长条状铝片的一端放在酒精灯火焰上灼烧片刻,轻轻摇动铝条,受热一端会左右摇晃,却不像蜡烛那样滴落。为究其原因,小芳查阅资料得知:铝的熔、沸点分别是
请解释上述实验现象: 。
四、计算
20.(6分)为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品l
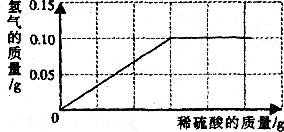
(1)样品中铜的质量分数;
(2)反应所消耗的硫酸溶液质量;
(3)反应后所得溶液质量。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com