
2007-2008学年度第一学期期中考试九年级化学试题
(时间90分钟,满分100分)
可能用到的相对原子质量:H―
一、选择题(本题包括20小题,每小题2分,共40分。每小题只有一个答案正确,多选、错选均不得分)
1.将生活中常用的下列物质分别加入到水中,不能形成溶液的是( )
A.白糖 B.白醋 C.食用油 D.食盐
2.各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂具有乳化功能的是( )
A.用汽油除去衣服上的油污 B.用餐具洗洁精清洗餐具上的油污
C.用水洗去盘子中的水果渣 D.用醋洗去水壶的水垢
3.用氯化钠固体配制

A.②④⑥⑦ B.①④⑤⑥ C.①③⑤⑦ D.①③④⑥
4.炎热的夏天,小林打开冰箱,从
A.
B.室温下,b溶液一定是饱和溶液
C.蔗糖晶体的溶解度随温度的升高而降低
D.a溶液的溶质质量分数大于b溶液的溶质质量分数
5.
A.该溶液中溶质的质量等于
C.该溶液中溶质的质量分数等于36% D.加水后该溶液变为不饱和溶液
6.下列关于溶液的说法错误的是( )
A.饱和溶液析出晶体后,其溶质的质量分数可能不变
B.在溶液里进行的化学反应,通常比较快
C.同种溶质的饱和溶液,一定比它的不饱和溶液的溶质质量分数大
D.不饱和溶液转化为饱和溶液,溶质质量分数可能不变
7.下图表示M、N两种固体物质的溶解度曲线。下列说法正确的是( )
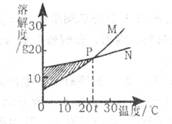
A.
C.P点表示t℃时M、N的溶解度相等 D.阴影处M、N均为饱和溶液
8.医院里常用溶质分数为5%的双氧水(H2O2)溶液清洗受伤病人的伤口,若要配制5%的双氧水溶液
A.
9.将少量的生石灰加到一定质量的饱和石灰水中,溶液的温度升高,再恢复到室温(不考虑水的蒸发)。下列四位同学对变化后溶液的分析错误的是( )

10.下表是
溶液中溶质的质量分数
4%
12%
16%
24%
28%
硫酸溶液的密度(g/ml)
1.02
1.08
1.11
1.17
1.20
氨水的密度(g/ml)
0.98
0.95
0.94
0.91
0.90
A.质量分数为28%的硫酸加入等质量水,所得溶液的密度小于
B.质量分数为24%的硫酸加入等体积水,所得溶液的密度大于
C.质量分数为28%的氨水加入等质量水,所得溶液的质量分数不等于14%
D.质量分数为24%的氨水加入等体积水,所得溶液的密度等于
11.用氯化钠配制
A.①②③④ B.⑤②④① C.①③⑤②④① D.①③⑥⑤②④①
12.2008年北京奥运会吉祥物――“福娃”向世界传递着友谊、和平、积极进取的精神。为儿童安全考虑,有一种“福娃”的外用材料为纯羊毛线,内充物为无毒的聚酯纤维。下列说法正确的是( )

A.羊毛的主要成分为纤维素 B.这种“福娃”不宜用碱性强的洗涤剂清洗
C.聚酯纤维是天然材料 D.不可以用燃烧的方法区分羊毛和聚酯纤维
13.室内装潢和家具挥发出来的甲醛是室内空气的主要污染物,甲醛易溶于水,常温下有强烈刺激性气味,当温度超过
A.入住前,房间内应保持较高温度并通风 B.选择在温度较高的季节装修房间
C.检测室内甲醛含量低于国家标准后再入住 D.紧闭门窗一段时间后再入住
14.化学是材料科学、生命科学、环境科学和能源科学的重要基础。下列有关说法正确的是( )
A.合金、合成纤维、合成橡胶、塑料都是有机高分子材料
B.香烟、酒精、吗啡、海洛因都是毒品
C.二氧化硫、二氧化氮、一氧化碳都是大气污染物
D.石油、煤、天然气、氢气都是不可再生的化石燃料
15.《京都议定书》是国际社会为防止全球气候变暖,控制温室气体排放的一项国际合约。其中的温室气体主要是指( )
A.二氧化碳 B.水蒸气 C.氢气 D.氧气
16.我国古代工艺品中不是以无机非金属材料为主要原料的是( )
A.青铜器 B.唐三彩 C.紫砂壶 D.宋代瓷器
17.作为2008年北京奥运会足球比赛的分赛场,沈阳奥体中心体育场宛如水晶皇冠般璀璨地闪耀在浑河南岸。场馆建设中使用了大量的钢筋,下列有关钢筋的说法中不正确的是( )
A.钢筋是混合物 B.钢筋属于金属材料
C.钢筋的韧性优于生铁 D.钢筋混凝土就是钢筋和混凝土的合成材料
18.保护环境,提高环保意识是每个公民的义务和责任。为了改善我们的生存环境,下列几项措施你认为切实可行的是( )
①推广使用标有CNG(压缩天然气)的公交客车 ②将废旧电池深埋地下 ③控制烟花爆竹的燃放 ④垃圾分类回收 ⑤控制生活污水和工业废水的任意排放( )
A.只有①②④ B.只有①③④⑤ C.只有①③⑤ D.只有②③④⑤
19.据报道,江西南昌被美国《新闻周刊》评选为2006年“全球十大最有活力的城市”,这将掀起又一轮南昌投资热。为避免投资办厂引起的环境污染,下列措施可行的是( )
A.对工厂的烟囱加高处理 B.工厂废水直接排放
C.对工厂的固体废弃物进行无害化处理 D.化工厂建在居民区
20.“让化学走向公众”是全美化学周的口号。美国化学周活动主题的内容涉及化学的方方面面,但都与公众日常生活息息相关。你认为下列哪项内容不属于美国化学周活动主题( )
A.多彩的世界 B.食品化学 C.水电开发 D.地球及大气
二、填空与简答题(每空1分,共31分)
21.给溶液命名时,通常把________的名称放在前,把________的名称放在后。如把固体白磷溶于二硫化碳时,所形成的溶液叫做_______的_______溶液,其中_______是溶质,________是溶剂。
22.小刚同学绘制了如下图所示A、B两种固体物质的溶解度曲线。

(1)温度为t
(2)将A物质t
(3)我国有许多盐碱湖。湖中溶有大量的NaCl和Na2CO3,那里的人们冬天捞碱,夏天晒盐。据此我认为右图中(填字母) ________曲线与纯碱的溶解度曲线相似。
23.将下列各操作名称的序号填在后面的横线上(每个序号只填写一次):
①搅拌 ②蒸发 ③过滤 ④加热
(1)由饱和的食盐水得到食盐晶体_____________;(2)将饱和的硝酸钾溶液变为不饱和溶液____________.(3)除去食盐中的泥沙,先溶解,再____________。
24.以下图示中的甲、乙两图分别表示氯化钠在水中的溶解度曲线,丙图表示硝酸钾在水中的溶解度曲线,丁图表示氯化钠在某有机溶剂中的溶解度曲线。
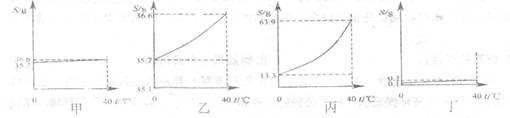
请将甲图分别与上述其它曲线对比,回答下列问题。
(1)由甲、丁得出:影响固体物质溶解度的因素是________________________。
(2)由甲、丙得出:影响固体物质溶解度曲线陡斜程度的因素是_______________________。因此欲除去硝酸钾中的少量氯化钠,可采用________________方法。
(3)由甲、乙得出________________________________________________________也会影响固体物质溶解度曲线的陡斜程度。
25.2005年国家质监局发布公告:禁止生产或进口有害的DEHA(C22H42O4)增塑剂的PVC食品保鲜膜。市场上保鲜膜的种类较多,要保证食品安全,必须注意识别。
(1)DEHA由__________种元素组成,分子中C、H原子个数比为__________。DEHA是一种____________ (填“有机物”或“无机物”),使用不当易通过食物进入人体。
(2)塑料保鲜膜不宜包装热的油炸食品,因为高温时保鲜膜中增塑剂分子更容易从保鲜膜进入食品中。从微观角度解释其原因是____________________________________。
(3)全世界每年生产、使用约上千万吨保鲜膜,使用后成为塑料垃圾,为了保护环境,你提出的一条合理化建议是____________________________________。
26.陶是人类最早利用化学反应制造的人造材料,青铜是人类最早利用化学反应制造的金属材料。陶器、青铜器及铝器的广泛使用,极大地促进了人类社会的发展。请回答下列问题:
(1)陶、铜、铁等材料的生产离不开火,火即所谓的燃烧,其实质是一种________________反应;而铜和铁的冶炼,主要是利用________________反应把铜和铁从其化合物中转化出来。
(2)制陶的原料是黏土,其主要成分是二氧化硅、氧化镁、氧化铝和碳酸钙。当温度达到
(3)在生产和生活中,大量使用的不是纯金属,而是它们的合金。合金与纯金属比较,其优越的性能有(答出一条即可________________________,原因是________________________。
(4)材料常常成为一个时代的标志,如陶器时代、青铜器时代、铁器时代。在信息时代,你认为对社会有重大影响的一种人造材料是____________________________。
(5)地壳中铝、铁的含量分别位列金属的第1和第2位,远多于铜,但铜却是人类最早冶炼出的金属,已有6000多年的历史,而冶炼铁比铜晚了3000多年,至于冶炼铝则只有二百多年的历史。根据金属的性质,你认为关键的因素是___________________________________
三、实验及探究题(每空1分,共17分)
27.某兴趣小组利用家中的材料研究影响物质溶解性的因素,实验步骤设计如下:
(I)称取一定质量的冰糖,研磨成粉末,每
(Ⅱ)按照下表进行实验(实验所需仪器略)
第一组
第二组
第三组
第四组
实验温度
固体种类
冰糖
冰糖
冰糖(粉末)
冰糖(块状)
冰糖
食盐
冰糖
固体质量
溶剂种类
水
植物油
水
水
水
水
水
溶剂质量
请你对他们的实验设计进行评价:
(1)根据上述的设计,你认为他们准备研究的影响因素包括__________________________,其中不会影响物质溶解性的因素是________________________________。
(2)在第一组、第三组、第四组的实验中使用研磨好的粉末状的冰糖而不使用块状冰糖的优点在于________________________________________________________________。
(3)你认为第四组实验的设计是否会影响实验结论的得出_________________;请简述理由__________________________________________________________________________。
28.下图是小明配制
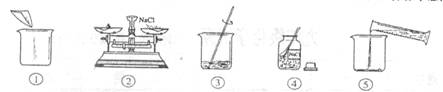
(1)配制过程中使用的四种玻璃仪器,分别是广口瓶、___________、__________、量筒。
(2)请你指出图中一处错误操作,并分析该操作可能造成的后果_________________________
(3)图②、图③表示的操作步骤分别是_______________________________________。
(4)配制时需称量氯化钠________g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数会_____________
(填“偏大”或“偏小”);量取水最好选择_____________量筒(填序号①10mL②50 mL③100mL)。(水的密度为
29.某同学为了探究废弃塑料薄膜混杂在土壤中对植物生长的影响,设计了如下实验:取两个同样的花盆,找5―8个废旧塑料袋,剪成小碎片,再取
(1)你估计,1个月后,二者的生长情况分别为_____________________________________。造成这种现象的原因是____________________________________________。
(2)在上述实验中,强调让两株植物在相同条件(温度、浇水、光照等)下生长。这样做的目的是__________________________________________________________________。
(3)你估计,在上述实验过程中。可能会出现什么意外情况影响实验的正常进行? __________________________________________________________________
(4)通过该实验,你能得到什么启示?你认为应向使用塑料薄膜做大棚或地膜的农民提出的建议为__________________________________________________________________。
四、计算题(12分)
相对分子质量:36.5
密度:
质量分数:36%
(1)欲配制14.6%的稀盐酸
(2)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com