|
试题详情
20.下表是20℃时硫酸溶液和氨水的密度与其溶质的质量分数对照表。下列说法正确的是 溶液中溶质的质量分数 4% 12% 16% 24% 28% 硫酸溶液的密度(g/mL) 试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
A.质量分数为28%的硫酸加入等质量水,所得溶液的密度小于1.08 g/mL 试题详情
B.质量分数为24%的硫酸加入等体积水,所得溶液的密度大于1.08 g/mL C.质量分数为28%的氨水加入等质量水,所得溶液的质量分数等于14% 试题详情
D.质量分数为24%的氨水加入等体积水,所得溶液的密度等于0.95 g/m 第Ⅱ卷(非选择题 共60分) 试题详情
三、(本题共4小题,每空1分,共20分) 21.(3分)在日常生活中应注意合理摄取营养物质和人体必需的元素。 (1)蛋白质是构成生命的基础物质,是日常膳食的重要组成部分。下列食物: ①苹果 ②葡萄干 ③牛奶 ④米饭 ⑤大豆 其中含有丰富蛋白质的是 (填写编号)。 (2)人体摄入的淀粉在酶的催化作用下与水作用最终变成葡萄糖,葡萄糖在酶的催化作用下经缓慢氧化转变成
,同时放出能量,供机体活动和维持恒定体温的需要。 (3)目前一种叫碘酸钙的保健品已进入一些超市,其含有人体必需的微量元素有 。 试题详情
22.(4分)我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质和用途,也需要寻求它们之间的内在规律性。为此,科学家根据元素的结构和性质,将它们科学有序排列成元素周期表的形式。下表是元素周期表中的一部分,表中的元素是人体生命活动的常量元素。 试题详情

试根据上表回答下列问题: (1)氮元素的核电荷数x =
。 (2)与钠元素化学性质相似的元素为
。 (3)氧、氯、硫、磷在化学反应中一般易
电子,趋向达到相对稳定结构。 (4)分析上表可发现:每一横行元素从左向右排列所遵循的一条规律是
。 试题详情
23.(5分)已知A、B、C三种固体含有同种金属元素,A难溶于水,B是一种氧化物,可作干燥剂。D、E、F含有同种非金属元素,E是常见的固体单质,D、F通常状况下为气体。X由两种元素组成,其中E元素的质量分数为37.5%,与另一种元素原子个数比为2∶1。它们的转化关系如下图(部分产物已略去)。 试题详情
 
(1)写出E、X物质的化学式:E ; X
。 (2)写出C→A的化学方程式:
____________________________________。 (3)实验室若分离由D和F组成的混合气体,如采用上图装置,则a中应盛有
(填写试剂名称,下同),b中应盛有
。 试题详情
24.(8分)实验中学同学开展复分解反应研究性学习,设计了如下研究性学习思路: 【练习质疑】下列各组物质间均能反应,写出③、④反应的化学方程式。 ①氢氧化钠溶液与盐酸 ②碳酸钠溶液与硫酸 ③硫酸铜溶液和氢氧化钠溶液
。 ④碳酸钠溶液和氯化钡溶液
。 【研究讨论】上述反应为什么能够发生?是因为这些反应物中含有特殊的阴、阳离子,如①中有H+和OH- ,②中有H+和CO32-,③中有
,④中有
。 【构建网络】按照一定的顺序排列这些离子,就可以形成一种网络形式。在网络中,用短线相连的这些阴、阳离子能两两结合生成沉淀或气体或水。现有Ca2+、SO42-、NH4+,请将它们填入下面合适的“( )”中,使其形成一个更为完整的复分解反应网络。 试题详情

【拓展运用】通过形成的网络,可以判断化合物间能否共存,进行物质的鉴别,用于物质的除杂等。如硫酸钠溶液混有硫酸铵,可以加入
(填写化学式)除去硫酸铵。 试题详情
四、(本题1小题,每空1分,共11分) 25.(11分)金属材料是现代生活和工业生产中应用极为普遍的一类物质。 (1)钛合金是21世纪的重要材料,具有熔点高、可塑性好、抗腐蚀性强、与人体有很好的“相容性”等优良性能。金属的下列用途:①用来做保险丝 ②用来制人造骨 ③用于制造船舶 ④用于制造航天飞机。其中与钛合金性能符合的是 (填序号)。 (2)铁是一种最主要的金属材料,实验室里用一氧化碳还原氧化铁得到铁,实验过程中,先通入一氧化碳目的是
。炼铁厂常以焦炭、赤铁矿、空气等为主要原料炼铁,反应过程如下: 试题详情

写出② ③两步的化学方程式
、
。 (3)矿物的储量有限,而且不可再生,我们必须保护金属资源并进行金属的回收利用。某兴趣小组同学欲从含有硫酸、硫酸亚铁和硫酸铜的废液中,回收全部金属铜,应先加入
,反应的化学方程式为:
、
。充分反应后过滤,滤渣中含有
。继续处理可以得到纯净的金属铜和硫酸亚铁固体。 (4)在学习了金属资源保护内容以后,兴趣小组同学对金属的锈蚀做了观察,发现残留水的铁锅在与水面接触的部位最易生锈;家用的铜质水龙头也生了一层绿色的铜锈。回忆已有的知识,铁生锈的原因是
。那么铜生锈的原因是什么?查阅有关资料:铜锈的主要成份是Cu2(OH)2CO3。他们除依照铁钉锈蚀条件的探究方法进行实验外,还补充做了铜锈蚀与
有关系的实验。请写出一种防止铁或铜等金属制品生锈的具体方法 。 五、(本题共3小题,每空1分,共19分) 试题详情
26.(3分)正确的基本实验操作是确保实验成功和安全的前提。试回答: (1)量液时,量筒必须放平,视线
。 (2)用漏斗过滤时,注意液面始终要
。 (3)稀释浓硫酸时,切不可将
。 试题详情
27.(8分)请结合下列实验常用装置,回答有关问题。 试题详情
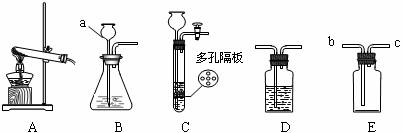
(1)写出图中标有字母的仪器名称:a__________。 (2)若用高锰酸钾制取氧气,应选用的发生装置是__________(填“A”、“B”或“C”),在加入药品前,应首先
,反应的化学方程式是
。 (3)若要制取二氧化碳,在B装置中装有石灰石,那么a中应加入___________。若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放
(填写试剂名称)。如果用E装置收集该气体,则气体从_________端进入(填“b”或“c”)。 (4)实验室如用块状固体和液体无需加热制取气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其优点是
。 试题详情
28.(8分)物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象。某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。 方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应。 (1)用pH试纸测定溶液的pH时,正确的操作是:
。 (2)简述强调“测得的pH小于7”的理由:
。 方案二:先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应。 该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞溶液,溶液变成了红色,过了一会儿红色就消失了。该小组对这种意外现象的原因作了如下猜想: ①可能是酚酞溶液与空气中的氧气反应,使红色消失; ②可能是氢氧化钠溶液与空气中的二氧化碳反应,使红色消失。 (1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液。实验中“加热”和“滴入植物油”目的是
。实验结果表明酚酞溶液红色消失与空气中的氧气无关。 (2)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论: 结论1:说明Na2CO3溶液呈
性; 结论2:说明酚酞溶液红色消失与空气中的二氧化碳无关。 (3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象。请设计实验证明该方案中取用的NaOH溶液浓度过大:①实验方法
,②观察到的现象
。 方案三:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。 该组同学将不同浓度的盐酸和NaOH溶液各10 mL混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表)。 试题详情

(1)表中x = 。 (2)某同学在没使用温度计的情况下,通过下图所示装置完成了实验。则该同学根据
判断NaOH溶液与稀盐酸发生了中和反应。 试题详情

六、(本题共2小题,共10分) 试题详情
29.(4分)铁是人类不可缺少的微量元素,正常人每天应补充14 mg左右的铁,其中大部分来自于食物。如果全部通过服用含FeSO4?7H2O的片剂补充铁,则每天约需要服用含___ mg FeSO4?7H2O的片剂。 试题详情
市场上某硫酸亚铁片剂,其中Fe2+的含量为16.0%。该片剂中的Fe2+在空气中易变质,国家规定该片剂中Fe2+变质超过10.0%即不能再服用。为检验某药店出售的硫酸亚铁片剂是否失效,取10.0
g该片剂经测定含Fe2+ 1.52 g。通过计算说明该片剂是否能服用? 试题详情
30.(6分)海洋约占地球表面积的71%,具有十分巨大的开发潜力。苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料。下图是我市某盐场苦卤中部分成分含量柱形图。试计算: (1) 若使100 g该苦卤中的MgCl2和MgSO4完全转化为Mg(OH)2沉淀,需要20% NaOH溶液多少克? 试题详情
 (2)将上述沉淀完全转化为无水MgCl2,并在熔融状态下进行电解,可得金属镁多少克?氯气多少升(该条件下氯气密度为3.0
g/L)? (2)将上述沉淀完全转化为无水MgCl2,并在熔融状态下进行电解,可得金属镁多少克?氯气多少升(该条件下氯气密度为3.0
g/L)?
试题详情
| 
