
2008年山东省济宁市中等学校招生考试
理科综合试卷化学部分
可能用到的相对原子质量:
H―
第I卷(选择题共16分)
选择题(下列各题只有一个正确选项。其中,11―14小题各1分,15―20小题各2分,本大题共16分)
11.王安石在《 咏梅》 中写到“墙角数枝梅,凌寒独自开。遥知不是雪,为有暗香来”。诗中的“暗香来”表明
A.分子很小,但真实存在 B.分子之间有一定的间隔
C.分子是不断运动的 D.分子是由原子构成的
12.根据特点对不同物质进行比较、分类是化学学习的重要方法之一。下列物质中,其名称、化学式和属类都正确的是
A.干冰一H2O一氧化物 B.水银一Ag一金属单质
C.碳酸气一H2CO3一酸 D.灰锰氧一KMn4一盐
13.鱼胆中含有胆汁酸(一种酸),它味苦、难溶于水。家庭做鱼的时候,不小心将鱼胆刺破,会使鱼肉沽上胆汁酸,影响鱼味道的鲜美。消除这种苦味,可用下面那种溶液冲洗
A.食盐水 B.食醋 C.纯酒溶液 D.饮用白酒
14.
A.C3H8是一种有机化合物
B.C3H8由C、H 两种元素组成
C.C3H8中C 、H 两种元素的质量比是3 : 8
D.C3H8分子中C 、H 两种元素的原子个数比是3:8

15.小红同学为证明某硝酸钾溶液是否达到饱和状态设计了以下方案。一定能达到目的的是
A.温度不变,向溶液中加人少量硝酸钾溶液
B.温度不变,向溶液中加人少量硝酸钾晶体
C.给溶液加热,直至有硝酸钾晶体析出
D.给溶液降温,直至有硝酸钾晶体析出
16.除去下列物质少量杂质(括号内为杂质)的方法中,正确的是
A.CO2(HCl)混合气体通过澄清石灰水后干燥
B.CuO(炭粉)混合物中滴加稀盐酸后过滤、烘干
c.Nacl溶液(CaC12)混合物中滴加适量碳酸钠溶液后过滤
D.NaoH溶液(Na2Co3)混合物中滴加适量氯化钙溶液后过滤
17.下列化学反应方程式书写正确且有共同特点的是
①  ↑ ②
↑ ② ↑
↑
③ ④
④
⑤ ⑥
⑥
A.①⑤ B.②③ C.④⑥ D.⑤⑥
18.日常生活、工农业生产和科学实验中,需要利用中和反应原理来降低某些环境中酸或碱的含量。学校课外活动小组利用5%的氢氧化钠溶液逐滴滴加到10mL5%的稀盐酸中,将测得溶液pH的变化绘制成下图所示曲线。分析曲线得到的以下说法中,合理的是

A.滴入少量氢氧化钠溶液,溶液呈酸性,pH = 0
B.滴入过量氢氧化钠溶液,溶液显碱性,pH=14
C.滴入适量氢氧化钠溶液至恰好反应,溶液呈中性,pH=7
D.未滴入氢氧化钠溶液时溶液显酸性,滴入氢氧化钠溶液后溶液显碱性
19.为探究不同金属的活动性顺序,一同学利用X、Y、Z三种金属的单质、稀盐酸和金属Y、Z的硝酸盐溶液进行下面实验,实验结果记录如下(“+”表示能反应,“一”表示不反应,无标识表示未进行实验)。则x 、Y 、z 三种金属的活动性顺序为

A.X > Y > Z B.Y >X>Z C.Z > X > Y D.Y >Z>X
20.课外探究小组为鉴别KCl、K2Co3 、K2SO4三种物质的溶液,设计了下面的实验方案。按此方案,他们在实验中要用到的两种试剂是

A.试剂甲:氧化钙,试剂乙:澄清石灰水 B.试剂甲:硫酸铜,试剂乙:硝酸银
C.试剂甲:稀盐酸,试剂乙:氯化钡 D.试剂甲:氢氧化钡,试剂乙:硫酸铜
第Ⅱ卷(非选择题共34 分)
一、填空与简答(共17 分)
1.(4分)从①氢气②氮气③干冰④氧化钙⑤甲烷⑥石灰石中选择合适的物质填写下面空格(填序号):
(l)可用于食品包装保护气的是 ;
(2)可用作无污染高能燃料的是 ;
(3)可用于制作舞台云雾景象的是 ;
(4)可用作工地建筑材料的是 。
2.(3分)下列符号中数字“
(1)H2SO4 ;
(2)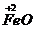 ;
;
(3)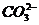 .
.
3.(3分)实验室少量制取硫酸铜有多种方法。可直接利用碎铜屑与浓硫酸共热制取[原理是: ],因反应中产生的二氧化硫气体有毒,污染室内环境,我们通常用碎铜屑与稀硫酸经几步反应来获取硫酸铜。请写出你的设计思路(用化学方程式表示,用到的其他简单物质可自己补充): .
],因反应中产生的二氧化硫气体有毒,污染室内环境,我们通常用碎铜屑与稀硫酸经几步反应来获取硫酸铜。请写出你的设计思路(用化学方程式表示,用到的其他简单物质可自己补充): .
对比以上两种方法,你所设计方法的优点是 .
4.(4分)下图是A、B两种固体物质的溶解度曲溶解度线。请分析曲线中A、B两种物质溶解度随温度的变化情况后,回答下面问题:
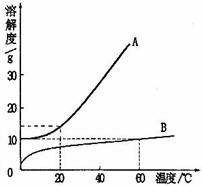
(1)我们一般将
(2)比较A、B两种物质的溶解度曲线,可看出A、B两物质溶解性的共同点是 ;
(3)有同学认为“同一温度时,可配得质量分数相同的A、B两种物质的饱和溶液”。你的观点是 理由是 。
5.(3分)甲、乙两组同学在探究物质的性质实验时,得到的废液中共含有K+、Ba2+、Cu2+、OH―、NO3―、CO32―六种离子。经测试:甲组同学实验所得废液的pH = 13;那么,乙组同学实验废液中含有的离子是 .经合作讨论,甲、乙两组同学将实验产生的废液按适当比例混合后,可将废液中对环境污染较为严重的Ba2+、Cu2+、OH―离子除去。请写出废液混合后发生的任意两个反应的化学方程式:① ,②
二、实验与探究(共11 分)
6.(1) (7分)下图是我们在实验室制取物质和进行物质性质实验的常用装置。请按要求回答下面的问题:
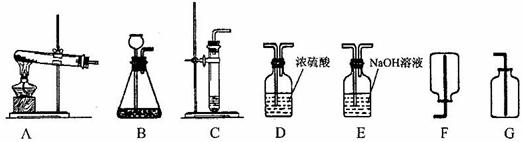 ① ①检查装置B气密性的方法是
,
① ①检查装置B气密性的方法是
,
②若在实验室中制得一瓶氧气,你选择的化学反应是 _ (化学方程式表示),选用的装置是 。
③使用锌和稀盐酸制取氢气,可选用的发生装置有 (填序号),产生的气体经装置 (填序号)分别除去少量的 和 后,即可得到纯净干燥的氢气。
(2) (4分)二氧化锰对许多化学反应都有催化作用。小明同学在完成某实验后,发现用作催化剂二氧化锰的颜色、状态均未发生明显变化,为进一步探究这时的二氧化锰是否仍有催化作用,小明将其分离回收,并想通过实验进行探究。请你帮他设计实验并回答下面问题:
①简述你的实验方法 ,
②在该实验中观察到的现象是_ _ _ __ _ _ _ _ _ ;
③根据实验现象,你得到的结论是 .
④通过探究,你对催化剂的认识是 。
三、计算与应用(共6分)
7.(2分)木糖醇(C5H12O5)是一种具有营养价值的甜味物质,也是人体糖类代谢的中间体。健康的人,即使不吃含有木糖醇的食物,血液中也含有0.03~0.06mg/100mL的木糖醇。木糖醇广泛存在于各种水果、蔬菜中,但含量很低。商品木糖醇是用玉米芯、甘蔗渣等农业作物经深加工而制得的,是一种天然健康的甜味剂。请采集信息回答下面的问题:
(l)木糖醇的相对分子质量为 ;
(2)醇的标志是其分子结构中含有经基(―OH) ,木糖醇中最多含有 个经基。
8.(4分)课题小组为测定某石灰石样品中CaCO3的含量,取
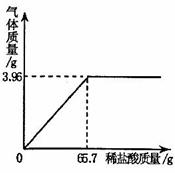
(l)样品中CaCo3的含量是多少?。(2)所用稀盐酸的质量分数是多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com