
期末测试A卷
测试时间:120分钟 总分:100分
一、选择题(每题1分,共30分)
1.奠定近代化学基础的是 ( )
A.原子论和分子学说 B.火的发明和利用
C.元素周期律 D.纳米技术的发明和使用
2.下面使用酒精灯的操作中,正确的是 ( )
A.向酒精灯中添加酒精,不超过酒精灯的
B.可以直接向燃着的酒精灯中添加酒精
C.熄灭酒精灯,一般用嘴来吹灭
D.为了下次使用方便,酒精灯不用时可不盖灯帽
3.使人类生存条件得以改善的主要因素是 ( )
A.黑火药的发明 B.酒的配制
C.火的发现和利用 D.纳米技术的使用
4.如下图所示的实验操作中正确的是 ( )

5.在装有空气的密闭容器中,欲用燃烧的方法除去其中的氧气,又不混入其他气体,可以使用的可燃物是 ( )
A.木炭 B.红磷 C.硫 D.蜡烛
6.下列对空气的描述不正确的是 ( )
A.按质量分数计,空气中含氧气21%,含氮气约78%
B.空气的成分是比较固定的
C.空气的成分以氮气和氧气为主
D.除氮气和氧气外,空气中还有约占1%的其他气体,且主要是二氧化碳和水蒸气
7.为了使灯泡经久耐用,常向灯泡里面充的气体是 ( )
A.二氧化碳 B.氮气
C.氮气和稀有气体的混合气体 D.氮气和氧气的混合气体
8.下列四种物质中组成区别于其他三种的一种物质是 ( )
A.空气 B.氮气 C.稀有气体 D.人呼出的气体
9.我国淡水资源紧缺,所以在生产和生活中应该 ( )
A.减少饮用水
B.将用过的废水、污水直接排放到江河湖海中重复利用
C.既要预防和消除对水源的污染,又要节约用水
D.不需开发水资源,因为水有巨大的自净能力
10.关于液态氧与氧气的说法,下列正确的是 ( )
A.它们的物理性质相同 B.它们的化学性质不同
C.它们由同种分子构成 D.它们是不同的物质
11.下列水的性质,属于化学性质是 ( )
A.在通常情况下,1L水中只能溶解大约30mL氧气
B.水是无色无气味的
C.水在直流电作用下可得到氢气和氧气
D.水在1.01×105Pa下冷却至0℃可结成冰
12.下列净化水的操作中,净化程度最高的是 ( )
A.静置沉淀 B.蒸馏 C.过滤 D.吸附沉淀
13.在原子中,决定相对原子质量大小的主要微粒是 ( )
A.质子数和中子数 B.质子数和电子数
C.中子数和电子数 D.核电荷数和电子数
14.人体中化学元素含量的多少,会直接影响人体健康,下列元素中,因摄入量不足容易导致人患骨质疏松症的是 ( )
A.铁 B.碘 C.钙 D.锌
15.原子核外有11个电子的某种原子,假如它失去一个电子后,剩余部分 ( )
A.不显电性 B.显正电性 C.显负电性 D.无法确定
16.燃放烟花爆竹能产生一种有刺激性气味的气体,会污染空气。该气体由两种元素组 成,其质量比为1:1。这种气体是 ( )
A.H2S B.SO2 C.CO D.NO2
17.元素氢、氧和X的化合价分别是+1、-2、+6,这三种元素组成的化合物的化学式可能是 ( )
A.HXO B.H2XO4 C.H2XO3 D.HXO3
18.根据化学方程式;3AB+C2B3==2C+3X,可确定X的化学式是 ( )
A.A3B2 B.A2B3 C.AB2 D.AB3
19.下列关于质量守恒定律的说法中,正确的是 ( )
A.化学反应前后,反应物的分子总数一定等于生成物的分子总数
B.化学反应的实质就是分子之间的重新组合
C.参加化学反应的各物质的总质量一定等于反应后生成的各物质的总质量
D.对于有气体参加的化学反应,反应前后的体积一定不变
20.在A+B==C+D的反应中,已知30gA和10gB恰好完全反应,生成5gD,且已知C的相对分子质量为70,则A的相对分子质量是 ( )
A.20 B.25 C.40 D.60
21.在化学方程式 C3H8+bO2
C3H8+bO2 CO2+
CO2+ H2O中,各化学式前化学计量数之间的关系正确的是 ( )
H2O中,各化学式前化学计量数之间的关系正确的是 ( )
A. B.
B. C.
C.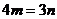 D.
D.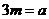
22.用墨书写的字或绘的画能保存多年不褪色,是由于常温下碳 ( )
A.化学性质不活泼 B.具有吸附性
C.具有还原性 D.具有氧化性
23.下列关于碳的几种单质的组成和用途说法错误的是 ( )
A.活性炭可用作防毒面具的滤毒剂
B.铅笔芯主要是用铅和少量炭粉制成的
C.长期未用而难开启的铁锁,可在锁孔中加入少量的铅笔芯粉便于开启
D.璀璨夺目的天然钻石是由碳元素组成的
24.下列叙述不正确的是 ( )
A.矿物燃料在地球上的蕴藏量并不是无限的
B.煤和石油只要完全燃烧就不会造成对空气的污染
C.人类必须节约现有的能源,并大力开发新能源
D.对煤和石油要合理开发,综合利用
25.氢气作为新型燃料的主要优点是 ( )
A.燃烧放出的热量高,且无污染 B.易保存,使用安全
C.易点燃,资源丰富 D.比空气轻,难溶于水
26.海湾战争期间,科威特大批油井被炸起火燃烧,我国救援人员在灭火工作中作出了贡献。下列措施中不能考虑用于油井灭火的是( )
A.设法阻止石油喷射 B.设法降低油井井口的温度
C.设法降低石油着火点 D.设法使用火焰隔绝空气
27.3g木炭和5g氧气在密闭容器中完全反应,下列叙述中正确的是 ( )
A.产物全部是CO B.木炭过量,产物为CO
C.产物全部是CO2 D.产物中有CO,也有CO2
28.实验室用简易发生装置制取二氧化碳并验证二氧化碳的性质时,有以下几步操作,正确的顺序为 ( )
①向试管中装入大理石 ②检查装置气密性 ③向长颈漏斗注入酸液 ④连接装置
⑤向试管中倒入澄清石灰水 ⑥将产生的气体通入澄清石灰水
A.⑤④②①③⑥ B.②④⑤①③⑥
C.④②①③⑤⑥ D.④⑤②③①⑥
29.某有机物在空气中完全燃烧时,生成CO2和H2O的质量比为11:9,则该有机物可能是 ( )
①CH4 ②C2H2 ③C2H5OH ④CH3OH
A.①④ B.②③ C.①② D.①③
30.为探究植物光合作用的原理,某校学生设计了如下实验装置。在同样条件下,你预测数天后植物生长最茂盛的是 ( )
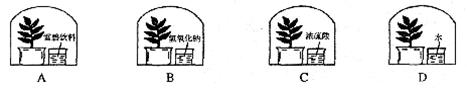
二、填空题(43分)
31.(2分)已知硫酸是由硫酸分子构成的,其化学式为H2SO4。现有符号“3H2SO4”,试说出其中数学“2、3”的意义:“2” ;“3” 。
32.(3分)露天烧烤不仅产生大量的有害气体污染环境,而且烧焦的肉类中还含有强烈的致癌物质3,4苯并芘,其化学式为C20H12,该物质的相对分子质量是 ,一个分子里共含有 个原子,碳、氢元素的质量比为 。
33.(6分)镁原子的结构示意图如下图所示,其中圆圈“○”表示 ,圈内“12”表示 ,圆弧“)”表示 ,由此该原子共有 个电子层,最外层上有 个电子,化学反应中易 (填“得”或“失”)电子。
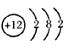
34.(8分)写出下列化学方程式。
(1)汽车尾气中含有的CO、NO等有害气可在用铂、钯作催化剂的条件下,使CO与NO反应生成绿色植物光合作用所需的一种气体和空气中体积分数最大的一种气体。
(2)为延长白炽灯泡的使用时间,灯泡内放有极少量的红磷,以减少灯丝氧化。
(3)镁带可以在二氧化碳中燃烧,生成炭黑(主要成分为碳)和镁的氧化物。
(4)我国自行设计和制造的长征3号火箭用液氧和液氢作推进剂,点火时发生反应。
19世纪末,物理学家瑞利在研究中发现,从空气中分离得到的氮气密度,与从含氮物质中制得的氮气密度有0.0064g/m3的差异。他没有放过这一微小差异,在化学家拉姆塞的合作下,经过十几年努力,于1894年发现了空气中的氩。
下列有关结论中,正确的是 ;(填序号)
①氩是一种化学性质极不活泼的气体 ②瑞利从空气中分离出的氮气是纯净物 ③19世纪末以前,人们认为空气由氧气和氮气组成 ④瑞利发现从含氮物质制得的氮气密度大于从空气中分离得到的氮气密度
36.(4分)某学生书写了如下化学方程式:A.KClO3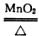 KCl+O2↑ B.C+O2
KCl+O2↑ B.C+O2 CO2↑ C.Mg+O2
CO2↑ C.Mg+O2 MgO2
D.3Fe+2O2
MgO2
D.3Fe+2O2 Fe3O4。其中(1)化学式写错的是(填序号,下同) ;(2)未配平的是 ;(3)“↑”用错的是 ;(4)反应条件写错的是 。
Fe3O4。其中(1)化学式写错的是(填序号,下同) ;(2)未配平的是 ;(3)“↑”用错的是 ;(4)反应条件写错的是 。
37.(4分)通过学习,我们初步认识到:化学反应快慢、现象、生成物和反应物的量的多少、反应条件有着密切的关系。请根据题意,各举一例说明:
(1)使用催化剂能改变化学反应速率 。
(2)反应物的量(浓度)不同,反应现象可能不同 。
38.(3分)最近两则新闻引起我省人民广泛关注:①2003年5月13日,安徽淮北芦岭煤矿发生特大瓦斯爆炸(瓦斯的主要成分是甲烷),造成重大伤亡。②2003年5月26日,中央电视台《新闻联播》报道,“西气东输”工程进展迅速,明年安徽等省市将用到质优价廉的天然气。
(1)请用化学知识分析瓦斯爆炸的原因: 。
(2)写出天然气燃烧的化学方程式: 。
(3)上面两个例子说明,化学物质可以造福人类,但有时也会给人类带来危害。请你再举出生活中的一种物质说明这个问题: 。
39.(3分)2003年,武汉市政府坚持取缔正三轮摩托车(俗称“电麻木”),原因之一是正三轮摩托车产生的大量尾气严重污染城市生态环境。据有关专家介绍,每辆正三轮摩托车产生的尾气远远超过小汽车的排放量。
某同学通过查阅资料,发现机动车尾气是由汽油等燃料不完全燃烧产生的,含有CO2、CO、SO2、氮氧化物,挥发性有机物、固体颗粒等物质。由此,该同学推测:汽油中含有碳以及少量的氮、硫等物质,汽油在燃烧过程中发生了如下化学反应:
2C+O2 2CO(不完全燃烧)
2CO(不完全燃烧)
C+O2 CO2(完全燃烧)
CO2(完全燃烧)
S+O2 SO2
SO2
(1)该同学的推测 (填“正确”或“不正确”)。理由是
。
(2)请提出一条用化学手段治理汽车尾气的合理化建议。
40.(8分)下表是核电荷数为3~18的元素原子的核外电子排布示意图:

(1)上表中每一横行的元素原子的核外电子排布的特点是 ;每一纵行的元素原子的核外电子排布的特点是 。
(2)若将氢、氮元素也排人上表。已知氮元素的核外电子排布为 ,可得到以下两种形式:
,可得到以下两种形式:

你同意第 种排列方式,针对氮元素说明你选择的理由是 。
三、简答题(4分)
41.保温瓶中装有液态空气,当打开瓶盖将一根燃着的木条置于瓶口向上方时,请问木条是燃烧得更旺还是熄灭?为什么?
42.森林火灾每年都给人民生命和国家财产带来巨大损失。如果发生森林火灾,请你帮助策划可行的灭火方案。针对森林防火你有什么合理建议?
四、实验题(15分)
43.根据下图,回答问题:

(1)该同学利用此装置制氧气,所用的药品是什么? 。
(2)指出标有序号的仪器名称:
a ;b ;c ;d ;e ;f 。
(3)除上述收集法,还可采用 。
(4)请写出此反应的化学方程式: 。
(5)收集气体时,有气泡则立即开始收集,会导致什么后果?欲收集纯净的氧气,应该什么时候开始收集?
(6)实验结束时,应先撤去导管,再熄灭酒精灯,为什么?
44.下图是高温下用过量的木炭粉还原氧化铁的实验装置图。

(1)根据B中发生的现象,可判断反应是否开始产生,则B中的试剂 。(填名称)
(2)a处排出的气体中,除没有排尽的空气和未被完全吸收的带有水蒸气的二氧化碳外,还一定含有少量 (填化学式)气体。
(3)酒精灯上加网罩的目的 。
五、计算题(8分)
45.空气中含有少量臭氧(O3)可以起到消毒、杀菌作用,但臭氧过量对人体有害。我国的空气质量标准对空气中臭氧的最高浓度(单位体积的空气中所含臭氧的质量)限值如下表所示:
浓度限值/mg?m一3
一级标准
≤0.12
二级标准
≤0.16
三级标准
≤0.20
臭氧与KI溶液反应,生成一种可使带火星木条复燃的气体,反应后的溶液能使酚酞试液变红,也能使蘸有淀粉溶液的滤纸条变蓝。为测定某地空气中臭氧的含量,将50m3的空气通过足量的KI溶液,使臭氧完全反应;在所得溶液中再加入适量的硫代硫酸钠(Na2S2O3)溶液(含Na2S2O3的质量为47.4mg)恰好完全反应(2 Na2S2O3+I2== Na2S4O6+2NaI)。
(1)O3与KI溶液反应的化学方程式是 。
(2)通过计算确定该地空气中臭氧的浓度级别。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com