
2009年广东省中考模拟考试
化学试卷(十)
说明:本试题满分100分,考试时间80分钟。
选用的相对原子质量:H:1 S:32 Cl:35.4 O:16 Na:23 Ca:40
第一卷
一、选择题(本大题14小题,每小题2分,共28分。在每小题列出的四个选项中,只有一个是正确的)
1.下列物质中,属于纯净物的是
A.食醋 B.蒸馏水 C.空气 D.加碘盐
2.下列物质不属于有机合成材料的是
A.合金 B.塑料 C.合成橡胶 D.合成纤维
3.家庭中发生的下列变化,属于物理变化的是
A.蜡烛燃烧 B.天然气燃烧 C.水沸腾 D.菜刀生锈
4.毒奶粉是由糊精掺入一种三聚氰胺而成,关于三聚氰铵【化学式为C3N2(NH2)3】的说法正确的是
A.三聚氰胺中含有4种元素
B.三聚氰胺分子中碳氮原子个数比是1┱1
C.三聚氰胺中氮元素质量分数为60%
D.人体吸入过多三聚氰胺会形成肾结石疾病
5.下列物质的用途是利用其化学性质的是
A.稀有气体用于霓虹灯 B.金属铝制易拉罐
C.盐酸除铁锈 D.铜线制电缆
6.黄瓜富含维生素C,维生素C在pH<5的环境中较稳定,为减少维生素C的损失,在食用黄瓜时应加入少量的
A.食醋 B.纯碱 C.白糖 D.食盐
7.小明学习化学后,对抽烟的爸爸说:“吸烟有害健康,我和妈妈都在被动吸烟。”小明这样说的科学依据是
A.分子很小 B.分子在不断地运动
C.分子之间有间隔 D.分子是可分的
8.在学习过程中,总结规律要严谨、全面、科学。下列总结出的规律符合这一要求的是
A.酸溶液一定显酸性
B.某物质一定温度时的浓溶液一定是饱和溶液
C.含有氧元素的化合物一定是氧化物
D.有单质生成的反应一定是置换反应
9.下列物质中,蛋白质含量最高的是
A.白菜 B.大米 C.苹果 D.猪肉
10.下列有关钢的说法,错误的是
A.钢是含有少量碳及其他金属的铁 B.钢是金属材料
C.钢的性能优于生铁 D.钢不可能生锈
11.分类是学习和研究化学物质及其变化的一种常用的基本方法.家中必不可少的氯化钠与下列哪组属于同一类物质?
A.氢氧化铝、氢氧化钠 B.盐酸、硫酸
C.二氧化硫、二氧化碳 D.碳酸钠、硫酸铜
12.下列叙述中,错误的是
A.磷酸二氢铵(NH4H2PO4)是复合肥
B.CO2的大量排放会导致温室效应
C.图书档案、贵重设备、精密仪器等发生火灾时,可用泡沫灭火器扑灭
D.油污可以被洗涤剂通过乳化作用除去
13.下面是李好同学用连线的方式对某一主题知识进行归纳的情况,其中有错误的一组是
A.性质与用途
B.元素与人体健康
氢气燃烧产物为水――最理想的燃料
熟石灰呈碱性――改良酸性土壤
活性炭有吸附性――做净水剂
人体缺氟――易生龋牙
人体缺锌――影响人体发育
人体缺碘――甲状腺肿大
C.生活常识
D.环保与物质的利用
取暖防中毒――煤炉上放一壶水
防菜刀生锈――喷水后悬挂起来
海鲜品保鲜――甲醛水溶液浸泡
减少水污染――合理使用农药、化肥
减少汽车尾气污染――使用乙醇汽油
减少白色污染――使用可降解的塑料
14.下图中“――”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以转化为乙。下面四组选项中,符合下图要求的是

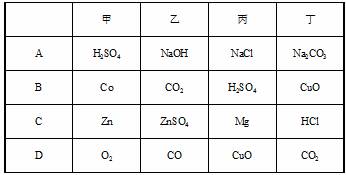
第二卷
二、填空题(本大题5小题,共20分)
15.(4分)生活离不开化学物质。现有以下五种物质:①生石灰、②食盐、③碳酸钙、④尿素、⑤酒精,请选择适当物质的序号填空:
(1)可用作火锅燃料的是__________。
(2)可用作补钙的盐是__________。
(3)可用作食品干燥剂的是__________。
(4)可用作氮肥的物质是__________。
16.(4分)人体胃液中含有适量的盐酸,可以帮助消化。胃液中pH值通常在0.9~1.5之间,超出这个范围会引起胃部不适。下面是两位胃病患者分别从医生处得到的药方的一部分:
病人甲
每日遵医嘱口服:
胃舒平【主要成分Al(OH)3】
病人乙
每日遵医嘱口服:
0.3%盐酸【主要成分HCl】
(1)甲病人所患的病可能是__________。
(2)乙病人服用的药,可用一种常见的调味品代替,这种调味品的名称是__________。
(3)写出胃舒平治病时发生的化学方程式:______________________________。
17.(5分)化学可以帮助人类认识、改造周周的世界,促进社会发展。
(1)糖类、油脂、蛋白质和维生素都是人类的基本营养物质。下表为某品牌燕麦片标签中的一部分。
每
糖类
油脂
蛋白质
维生素C
钙
镁
钠
锌
18 mg
201 mg
18.2 mg
30.8 mg
8.1 mg
①燕麦片的营养成分中能与水反应生成氨基酸的营养物质是__________,每克营养物质氧化时放出能量最多的是_________,人体必需的微量元素是_________;
②维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失。因此,烹调富含维生素C的食物时,应该注意__________。
(2)我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等。用灼烧法可初步鉴别三种纤维,给三种纤维编号后,分别灼烧产生的气味如下:
纤维编号
①
②
③
灼烧时的气味
特殊气味
烧纸气味
烧焦羽毛气味
则羊毛、棉花的编号分别为____________________。
18.(2分)把相同体积、相同质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如下图所示。这三种金属的活动性顺序为________;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为________。

19.(5分)火灾会给人们的生命财产带来巨大的损失,下面是小华同学对万一发生火灾时设计的灭火和自救应急方案:
①当火较小时,立即用各种灭火器材灭火;
②室内失火时,打开门窗,尽量让浓烟从门窗排出;
③在灭火过程中,用湿毛巾捂住口鼻;
④因煤气泄露引发火灾时,应先__________,再灭火。
请根据小华同学设计的灭火和自救应急方案,回答下列问题:
(1)在灭火和自救应急方案中,有一条不够妥当,该措施是________(填编号),理由是______________。
(2)在灭火过程中,用湿毛巾捂住口鼻,其中的道理是____________________。
(3)措施④中的空白应填____________________。
(4)在灭火措施中,少一条不可缺少的措施,该措施是____________________。
三、解答题(本大题2小题,共15分)
20.(7分)实验室有A、B两瓶溶液:A瓶是含有少量BaCl2的KCl溶液;B瓶是含有少量KCl的BaCl2溶液。小松和小思为回收试剂进行了如下实验探究。
(1)小松欲从A瓶中得到纯净的KCl晶体,可向A溶液加入稍过量的__________溶液,过滤后,在滤液中滴加盐酸至pH=7,再蒸发、结晶、烘干即得到纯净的KCl。
(2)小思欲从B瓶中得到纯净的BaCl2晶体,设计了如下的实验方案,请你填写以下部分实验报告:
(a)向B溶液中加入过量的碳酸钾溶液,其实验现象为____________________。
(b)过滤、__________(填“蒸发结晶”、“洗涤沉淀”或“冷却结晶”)。
(c)将(b)操作中得到的物质加入适量盐酸,其实验现象为_________________,反应的化学方程式为______________________________。
(d)将(c)操作中得到的滤液经蒸发、结晶、烘干即得到纯净的BaCl2。
21.(8分)在下面关系图中,A、B、C、D是初中化学中常见的单质,甲、乙分别是酒精燃烧时一定会产生的两种物质,丁是常用建筑材料的主要成分,G为无色有刺激性气味的气体,能使紫色石蕊变蓝,J是赤铁矿的主要成分。
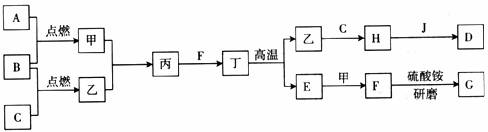
(1)写出化学式:甲是__________,G是__________。
(2)写出H与J反应的化学方程式:______________________________。
(3)J溶解于稀盐酸中,溶液呈黄色,反应完全后,再向溶液中加入纯净的D粉末,溶液逐渐变成浅绿色,写出有关变化的化学方程式:__________________________。
四、实验题(本大题2小题,共23分)
22.(11分)现有以下仪器,请回答下列问题:
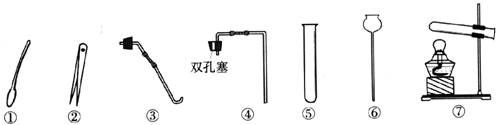
(1)仪器⑤的名称是__________;取用粉末状固体必须用到的仪器是__________(填序号)。
(2)如果用加热KMnO4的方法制取氧气,制气装置应选仪器__________(填序号)。
(3)如果用H2O2分解来制取氧气,制气装置最好选用仪器______(填序号);其化学方程式为:___________;这种装置还可以用来制CO2,其收集气体的方法为__________法。
(4)比较(2)和(3)两种制取氧气的方法,你认为较好的是______;原因是______________________________。
(5)把上面分解KMnO4制取氧气的仪器装配好后,检验该装置气密性的操作方法为:________________________________________。
23.(12分)某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止。为此,该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳。
【实验一】选择合适浓度的硫酸
操作:在
试管编号
1
2
3
4
5
硫酸浓度(%)
15
20
25
30
35
气体体积(mL)
35
47
55
51
42
【实验二】选择合适的反应温度
操作:往盛有
试管编号
A
B
C
D
E
温度(℃)
40
50
60
70
80
现象和比较
有少量气泡
气泡比A号试管多
气泡明显比B号试管多
大量气泡产生,与常温用盐酸反应相似
反应激烈,迅速产生大量气体
请根据本次活动的研究目的,分析处理以上两个表中的数据,得出结论:
(1)稀硫酸与大理石反应,在
(2)在合适的硫酸浓度下,应选择最合适的反应温度为__________℃,因为温度高于或低于该温度对反应的影响是______________________________。在最合适反应温度时硫酸与大理石反应的化学方程式为______________________。
(3)除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加____________________操作,更有利于气体的制备。
(4)你认为该研究小组还可以研究__________对该反应速率的影响。
(5)在以下硫酸和大理石反应的装置中,最佳选用__________(填编号)。
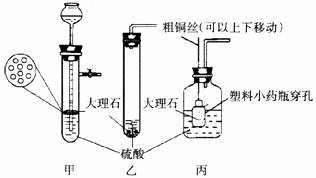
五、计算题(本大题2小题,共14分)
24.(7分)下表是某同学配成
实验序号
实验1
实验2
实验3
实验4
水的质量(g)
50
50
50
50
加入NaCl的质量(g)
30
40
50
60
所得溶液的质量(g)
80
100
105
(1)实验2所得溶液的质量为__________。
(2)四次实验中,实验__________所得的溶液属于饱和溶液,该饱和溶液质量分数是__________。
(3)实验3所得溶液
25.(7分)某同学为了测定黄铜屑(由锌和铜形成的合金)样品的组成,分四次取样品与稀硫酸反应,其实验数据记录如下表。
1
2
3
4
取样品质量(g)
50.0
50.0
50.0
50.0
取稀硫酸质量(g)
40.0
80.0
120.0
160.0
产生气体质量(g)
0.4
0.8
1.0
1.0
试计算:
(1)黄铜中锌的质量分数。(2)所用稀硫酸中溶质的质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com