
2009年淄博市博山初中毕业年级学业水平检测
理科综合试卷化学部分
注意事项:
1.答题前请考生务必在答题卡及试卷的规定位置将自己的姓名、考号、科目、座号(第11卷)等内容填写(涂)准确。
2.本试题分第一卷和第二卷两部分。第一卷为选择题,64分;第二卷为非选择题,116 分;共180分。考试时间为150分钟,考生不准使用计算器。
3.第一卷每小题选出答案后,必须用28铅笔把答题卡上对应题目的答案标号(A、B、C、D)涂黑,如需改动,须先用橡皮擦干净,再改涂其它答案。第二卷须用蓝黑 钢笔或圆珠笔直接答在试卷上。
4.考试结束后,由监考教师把第二卷和答题卡一并收回。
5.可能用到的相对原子质量:C l2 O16 Na23 S32 Cu64
第一卷(选择题共64分)
一、选择题(本题共42小题,每小题给出的四个选项中只有一个是正确的,请把正确的选项涂在答题卡的相应位置上。1―15题为生物部分,共20分;l6―30题为化学部分,共20分;31-42题为物理部分,共24分。)
16.诗词是民族灿烂文化中的瑰宝。下列著名诗句中隐含有化学变化的是①千里冰封,万里雪飘②白玉为床,金作马③野火烧不尽,春风吹又生④粉骨碎身浑不怕,要留清白在人间?⑤夜来风雨声,花落知多少⑥春蚕到死丝方尽,蜡炬成灰泪始干
A.①②③ B.②④⑤ C.③④⑥ D.③⑤⑥
17.20世纪以来,随着科学技术的迅速发展,能源的过度开发和消耗导致全球性的能源短缺和环境污染。从原料来源和对环境的影响考虑,下列能源中,最具开发前景的能源是
A.煤 B.石油 C.太阳能 D.天然气
18.蔬菜、水果可以调节身体健康,主要原因是蔬菜、水果中富含人体需要的
A.油脂 B.维生素 C.蛋白质 D.淀粉
19.人体内的一些液体的正常pH范围如下表,正常情况下,这些液体中一定呈酸性的是
血浆
乳汁
唾液
胆汁
胰液
胃液
pH范围
7.35~7.45
6.6~7.6
6.6~7.1
7.1~7.3
7.5~8.0
0.9~1.5
A.胃液 B.血浆 C.乳汁 D.唾液
20.某些食品包装袋内常有一小包物质,用来吸收氧气及水分,以防止食品腐败,常称“双吸剂”。下列物质属于“双吸剂”的是
A.炭粉 B.铁粉 C.氯化钙 D.生石灰
21.超导材料为具有零电阻及反磁性的物质,以Y2O3 、BaCO3和CuO为原料经研磨烧结可合成一种高温超导物质Y2Ba4Cu6Ox,假设在研磨烧结过程中各元素的化合价无变化,则x的值为
A.I2 B.
22.下列操作中,错误的是
A.用量筒取一定体积的溶液时,仰视读数或俯视读数
B.在实验室里制取O2、CO2气体时,应先检查装置气密性,再装药品
C.氢氧化钠沾到皮肤上,要立即用大量水冲洗,再涂上硼酸溶液
D.给试管里的液体加热,试管口不能对着自己或他人
23.人体口腔内唾液的pH通常约为7,在进食过程的最初10分钟,酸性逐渐增强,之后酸性逐渐减弱,至40分钟趋于正常。与上述事实最接近的图像是
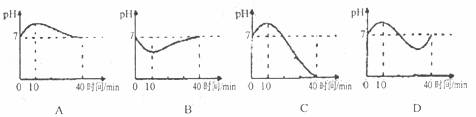
24.某同学为了区别氢氧化钠溶液和澄清石灰水,设计了如下图所示的四组实验方案,其中能达到目的的是
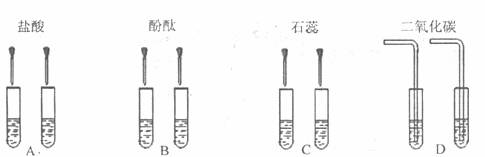
25.对下列实验过程的评价,正确的是
A.烧碱溶液中是否混有氯化钠,可先加稀盐酸,再加AgNO3溶液即可
B.某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含有SO42-
C.检验氢气纯度时,将试管口移近火焰,没有爆鸣声,表明氢气纯净
D.某无色溶液中滴入酚酞试液变红色,该溶液不一定是碱溶液
26.在学习化学的过程中,及时对所学知识进行整理,是一种好的学习方法。以下归纳中,有错误的是
A.化学知识中有许多的“相等”:
原子核中质子数与中子数相等
化合物中元素化合价的正价总数与负价总数的数值相等
稀释前后溶液中溶质的质量相等
B.相似物质(或微粒)之间的区别:
氯离子和氯原子――最外层电子数不同
二氧化硫和三氧化硫――分子构成不同
生铁和钢――含碳量不同
C.选择实验室制取气体装置与净化方法的依据
发生装置――反应物的状态和反应条件
收集装置――气体的性质,如:密度和溶解性
净化方法――气体及所含杂质的化!学性质
D.环境问题 主要原因 解决对策
温室效应――二氧化碳――减少化石燃料的使用
水质恶化――污水排放――先处理后排放
白色污染――塑料――开发使用可降解塑料
27.下列关于化学实验的“目的―4粱作一现象一结论”的描述正确的是
实验过程
组别
实验目的
所加试剂(或操作)
实验现象
实验结论
A
检验某混合气体中是否含有CO2气体
通入澄清石灰水中
无明显现象
该气体中不含CO2
B
除去KCl中的少量K2CO3
稀盐酸
有气泡产生
K2CO3已被除完
C
区分硬水和蒸馏水
肥皂水
产生大量泡沫
该液体为蒸馏水
D
用排空气法收集CO2时检验集气瓶中CO2是否集满
将燃烧的木条伸入瓶内
木条熄灭
瓶内CO2已集满
28.某农田出现土壤酸化板结现象,‘经调查,该农田长期施用化肥(NH4)2SO4,下列推测中错误的是
A.(NH4)2SO4溶液的pH可能小于7
B.土壤酸化板结可能是长期施用(NH4)2SO4的结果
C.为了防止土壤酸化,施用(NH4)2SO4的同时加入Ca(OH)2
D.草木灰(主要含K2CO3)可改良酸性土壤,说明K2CO3的溶液可能呈碱性
29.下图是KNO3和NaCl的溶解度曲线。下列说法中正确的是
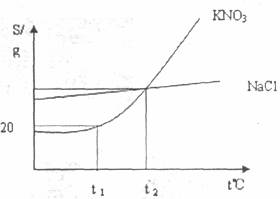
A.NaCl的溶解度不受温度的影响
B.tl℃时,
C.t
D.温度高于t
30.下边为甲( )与乙(
)与乙(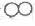 )反应生成丙(
)反应生成丙( )的微粒数变化示意图,则下列说法正确的是
)的微粒数变化示意图,则下列说法正确的是
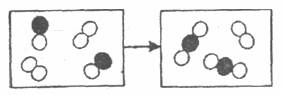
A.甲一定是氧化物 B.右框图的物质是纯净物
C.该反应类型是分解反应 D.甲、乙、丙的化学计量数之比为2:1:2
第Ⅱ卷(非选择题 共116分)
一、理解与应用(每空l分,共17分)
16.(3分)现有①四氧化三铁,②空气, ③铁粉, ④氯酸钾, ⑤液态氧, ⑥水,⑦氯化钾,⑧海水等物质,其中属于化合物的是_________;属于氧化物的是_________;属于混合物的是_______________。
17.(3分)某微粒结构示意图为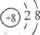 ,该微粒的符号是_____,它有_____个电子层,最外层电子数为___________。
,该微粒的符号是_____,它有_____个电子层,最外层电子数为___________。
18.(7分)燃烧与我们的生活与社会的发展有着密切的联系。
(1)下图是燃烧条件示意图:

请根据初中所学知识,写出燃烧的三个条件:
①__________________________________。
②________________________________。
③_________________________________。
(2)物质发生化学反应的同时,伴随着能量的变化,通常表现为___________变化。人类通过化学反应获得的能量,大多来自于化石燃料。石油是化石燃料之一,它属于(填“纯净物”或“混合物”)_______________。
(3)奥林匹克火炬(内部储有可燃物)是奥林匹克圣火的载体.
①采集奥林匹克圣火的唯一方式,是在奥林匹克的赫拉神庙前通过太阳光集中在凹面镜的中央,引燃圣火。此过程中最关键的燃烧条件是______________。
②北京奥运会火炬能在每小时65公里的强风和每小时50毫米雨量的情况下保持燃烧。但要实现奥运圣火登顶珠峰,还需要解决最关键的燃烧条件是____________。
19.(4分)去年8月奥运会在我国举行,奥运五环旗也将在北京飘扬。某校的化学兴趣小组制作了一面化学五环旗,如图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。常温下相连环物质问能发生反应,不相连环物质问不能发生反应,且B的相对分子质量大于D。请填空:
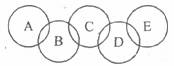
(1)写出下列物质的化学式:A_____________ D_______________
(2)相连环物质问能发生反应,按要求写出化学方程式。其中属下化合反应的是______。
(3)相连环物质间能发生的反应中,没有涉及的基本反应类型有_________。
二、实验与探究(共13分)
20.(6分)某课外兴趣小组,确立了“酸碱中和生成的正盐溶液的性质”作为研究课题,在研究中他们发现,正盐虽然不能电离出氢离子或氢氧根离子,但是其溶液却不一定呈中性,有的是酸性,有的呈碱性。为什么呢?盐溶液的酸碱性与什么有关呢?由“组成、结构决定物质性质”的观点出发,他们又进一步从组成特征上去找原因,发现正盐溶液的酸碱性与对应的酸和碱的强弱有关。他们将实验结果统计如下:
酸
碱
相应的正盐
溶液的pH
HCl(强酸)
NaOH (强碱)
NaCl
7
H2SO4(强酸)
KOH(强碱)
K2SO4
7
H2CO3(弱酸)
NaOH(强碱)
Na2CO3
>7
H3PO4(弱酸)
KOH(强碱)
K3PO4
>7
HNO3(强酸)
Cu(OH)2(弱碱)
Cu(NO3)2
<7
HCl(强酸)
Fe(OH)3(弱碱)
FeCl3
<7
(1)请你根据上表归纳出正盐溶液的酸碱性与对应酸、碱的强弱关系:
(2)根据他们的发现,请你判断硝酸钠、硝酸铁、硫酸铜、氯化钾、磷酸钠、碳酸钾六种溶液的酸碱性,其中溶液是酸性的是_______、呈碱性的是__________、呈中性的是_________。
21.(7分)巍巍午餐时买了一份菠菜和一份麻辣豆腐,但同学告诉她菠菜不能与豆腐同食。[发现问题]菠菜为什么不能与豆腐同食?[查阅资料]
a.制作豆腐需要加入石膏(主要成分:CaSO4):
b.菠菜中含有草酸、草酸盐等成分;
c.草酸钙是一种既不溶于水也不溶于醋酸的白色固体,是诱发人体结石的物质之一。
[提出猜想】菠菜与豆腐同食可能会产生人体不能吸收的沉淀物。
实验步骤
实验现象
实验结论
①将菠菜在少量开水中煮沸2~3min,取l~2mL滤液于试管中,并滴加少量_______溶液
产生白色沉淀
有草酸钙生成
②在步骤①的沉淀物中加入过量醋酸
沉淀部分溶解,且产生气泡
被溶解的沉淀一定不是________
[发现新问题]被溶解的沉淀是什么?产生的气体又是什么?于是她又设计如下试验进一步探究:
实验步骤
实验现象
实验结论
③将步骤②产生的气体通入__________中
产生的气体是________;步骤②被溶解的沉淀是碳酸钙
【反思与应用】
(1)家庭中常常将菠菜放在开水中煮沸2~3min捞出后再烹饪,其目的是________:
(2)联想到人体胃液中含有盐酸,请提出一个你想要探究的新问题:_____________ 。
三、分析与计算(本题6分)
22.星期天,小强的妈妈要焙制面包,叫小强取商店买回一包纯碱,小强仔细看了包装说明(如下图),并产生疑问:
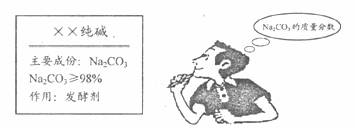
回到学校,他取出从家里带来的一小包纯碱样品进行实验:准确称取5.
(1)生成CO2的质量是_______:
(2)通过计算判断纯碱样品中碳酸钠的质量分数是否与包装说明相符。(计算结果精确到0.1%)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com