
江苏省通州市2009届高三第六次调研测试
化学试卷
(考试时间100分钟,满分120分)
说明:本试卷分第I卷和第II卷。请将第I卷选择题的答案用2B铅笔填涂到答题纸上。第II卷为非选择题,请将非选择题的答案写在答题纸上对应题号的答案空格内,直接写在试卷上无效。考试结束后,交回答题纸。
第Ⅰ卷(选择题 共48分)
可能用到的相对原子质量:H-
一、选择题(本题包括8小题,每题3分,共24分。每小题只有一个选项符合题意)
1.用于净化汽车尾气的反应:2NO(g)+2CO(g) 2CO2(g)+N2(g),已知该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是
2CO2(g)+N2(g),已知该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是
A.装有尾气净化装置的汽车排出的气体中不再含有NO或CO
B.提高尾气净化效率的常用方法是升高温度
C.提高尾气净化效率的最佳途径是研制高效催化剂
D.570K时该反应正向进行的程度很大,故使用催化剂并无实际意义
2.下列化学用语或模型图表示正确的是
A.甲烷的球棍模型: 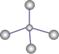 B.S2―的结构示意图为:
B.S2―的结构示意图为: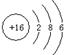
C.乙炔的最简式
CH≡CH
D.羟基的电子式 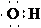
3.据最新报道,科学家发现了如下反应:O2+PtF6=O2 (PtF6),已知O2(PtF6)为离子化合物,其中Pt为+5价,对于此反应,下列说法正确的是
A.O2 (PtF6) 中不存在共价键
B.在此反应中每生成1mol O2 (Pt F6)则转移lmol电子
C.在此反应中,O2是氧化剂,PtF6是还原剂
D.O2 (PtF6)中氧元素的化合价是+l价
4.下列说法或表示方法正确的是
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由H+(aq)+ OH-(aq)= H2O(l) △H = -57.3 kJ?mol-1可知,若将含1 LpH=1的 CH3COOH溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ
C.由C(石墨)= C(金刚石) △H = +1.90 kJ?mol-1可知,金刚石比石墨稳定
D.在101 kPa时,
5.对于短周期元素,下列说法中正确的是
A.最外层电子数相同的元素一定位于同一主族
B.同一周期元素形成的简单离子的半径从左到右逐渐减小
C.若两种元素的原子序数相差8,一定是同一主族
D.同一主族的元素间也有可能形成离子化合物
6.在下列溶液中,各组离子可能大量共存的是
A.使pH试纸呈红色的溶液中:Fe2+、ClO-、SO42-、Na+
B.加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42-
C.由水电离出c(H+)=10-12 mol?L-1的溶液:K+、Al3+、Cl-、SO42-
D.在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
7.下列有关化工生产的叙述中正确的是
A.将煤液化、气化,有利于提高燃料的燃烧效率,减少污染物的排放
B.侯氏制碱法,向饱和NaCl溶液中先通入CO2再通入氨气制取纯碱
C.电解精炼铜时,同一时间内阳极溶解铜的质量与阴极析出铜的质量相等
D.工业生产硫酸中,建立高烟囱可以降低地面SO2的浓度,减少空气污染
8. v mL密度为g?mL的某溶液中,含有相对分子质量为M的溶质m g,该溶液中溶质的质量分数为W%,物质的量浓度为c mol?L,那么下列关系式正确的是
A.c=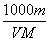 B.c=
B.c=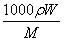 C.W%=
C.W%=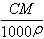 % D.m=
% D.m=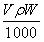
二、选择题(本题包括6小题,每小题4分,共24分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,若选错一个,该小题就为0分)
9. 根据下列实验现象,所得结论正确的是
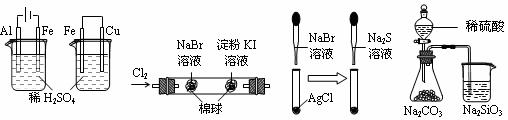
A. B. C. D.
实验
实验现象
结论
A.
左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡
活动性:Al>Fe>Cu
B.
左边棉花变为橙色,右边棉花变为蓝色
氧化性:Cl2>Br2>I2
C.
白色固体先变为淡黄色,后变为黑色(Ag2S)
Ksp:AgCl>AgBr>Ag2S
D.
锥形瓶中有气体产生,烧杯中液体变浑浊
非金属性:S>C>Si
10.设NA为阿伏加德罗常数,下列说法中正确的是
A.标准状况下,密度为d g/L的某气体纯净物一个分子的质量为g
B.常温常压下,
C.
D.
11.
A.0.1mol?L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H
B.Na2CO3溶液中:
C.NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:
c(Na+)>c(SO42-) >c(NH4+) >c(OH-) =c(H+)
D.pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液:
c(CH3COONa)>c(Na2CO3) >c(C6H5ONa ) >c(NaOH)
12.新鲜水果、蔬菜、果汁中富含的维生素C具有明显的抗衰老作用,但易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含量,用淀粉溶液作指示剂,其化学方程式为:
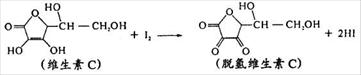
下列说法正确的是
A.上述反应为氧化反应 B.维生素C的分子式为C6H5O6
C.滴定时碘溶液盛放在碱式滴定管中 D.终点时溶液由蓝色恰好变无色
13.下列离子方程式的书写正确的是
A.实验室用浓盐酸与MnO2反应制Cl2:
MnO2 +4HCl(浓) Cl2↑+Mn2+ +2Cl-+2H2O
B.将标准状况下1.
2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
C.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:
Ca2++ HCO3- +OH- =CaCO3↓+H2O
D.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+H++ SO42- + NH4+ =BaSO4↓+ NH3?H2O +H2O
14.一定质量的Fe2O3、ZnO、CuO的固体混合粉末,在加热条件下用足量CO还原,得到金属混合物4.
A.50 mL B.100 mL C.200 mL D.缺少数据,无法计算
三、(本题包括1小题,共10分)
15.某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为沉淀可能是CuCO3;
乙同学认为沉淀可能是Cu(OH)2;
丙同学认为沉淀可能是CuCO3和Cu(OH)2的混合物。(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.(1)乙同学的观点,你认为其原理是 ▲ ;
(2)在探究沉淀成分前,须将沉淀从溶液中过滤、洗涤、低温干燥,检验沉淀是否洗涤干净的方法是 ▲ 。
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。
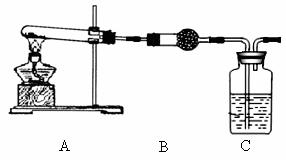
(3)B装置中试剂的化学式是 ▲ , C装置中试剂的名称是 ▲ 。
(4)能证明乙同学观点正确的实验现象是 ▲ 。
(5) 若丙同学的观点正确,用上述装置通过B、C中质量的增加来定量测定沉淀的组成,请你说说该装置主要存在的缺点 ▲ (至少二点)
四、(本题包括2小题,共18分)
16.(8分)下图是无机物A~H在一定条件下的转化关系(部分反应中参加反应的水未列出)。其中,A是一种带有结晶水的正盐,B是形成酸雨的主要物质,G是一种常见的二元强酸,E是一种红棕色粉末。
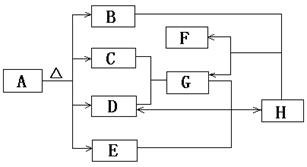
请填写下列空白:
(1)简述B形成的酸雨对环境的危害 ▲ ; ▲ (至少二点);
(2)配制F的溶液时要加 ▲ ;
(3)写出B+H→F+G的离子方程式 ▲ ;
(4)若A分解产生的B、C、D、E的质量比为16∶20∶63∶40,则A的化学式为 ▲ 。
17.(10分)如下图所示,在一定温度下,在一个容积为
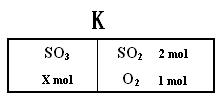
左室:2SO3(g) 2SO2(g) + O2(g) 右室:2SO2(g) + O2(g) 2SO3(g) △H=-197kJ/mol
回答下列问题:
(1) 能说明反应达到平衡的是 ▲ ;
A、隔板不再移动 B、左右二室SO2和O2物质的量之比相等
C、左右两边SO2的物质的量相等 D、左右二边SO3的体积分数相等
(2) 当X=0.5时,平衡后右室SO2的体积分数为a;X=1时,平衡后右室SO2的体积分数为b,则a和b的关系是 ▲ ;
A、a>b B、a=b C、a<b D、无法确定
(3) 若平衡时隔板在中央,则X= ▲ , 左室吸收的热量为Q1 kJ,右室放出的热量为Q2 kJ,则Q1、Q2间满足的关系是 ▲ ;
(4) 若将隔板固定在中央,且X=1,达平衡时右室的压强是起始时的0.7倍,则左室反应的平衡常数K= ▲ 。
五、(本题包括1小题,共10分)
18.铬(Cr)属于重金属元素,含铬废水和废渣排放必须经过处理达到有关的安全标准。
(1)含铬废水排放到河水中一定浓度会使鱼类等水生动物死亡的原因是 ▲ ;
(2)铬元素以Cr2O72-离子的形式存在于酸性废水中,常用FeSO4将其还原为Cr3+离子,再用沉淀法进行分离。
已知:
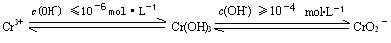
① FeSO4还原Cr2O72-的离子方程式为 ▲ 。
② Cr2 (SO4) 3溶液中加入过量NaOH浓溶液,反应的离子方程式为 ▲ 。
③ 沉淀法分离废水中的Cr3+离子,pH应控制在 ▲ 范围内。
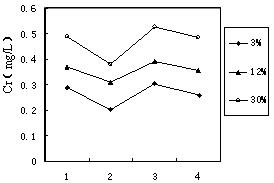 (3)铬冶炼工业的废渣粉碎后掺入煤矸石经过高温处理可以制砖,为了探究其中的铬元素在使用过程中是否会重新污染环境,研究组在一定条件下浸溶砖样,检测浸出液中Cr元素浓度,结果如图:
(3)铬冶炼工业的废渣粉碎后掺入煤矸石经过高温处理可以制砖,为了探究其中的铬元素在使用过程中是否会重新污染环境,研究组在一定条件下浸溶砖样,检测浸出液中Cr元素浓度,结果如图:
说明:1――用蒸馏水浸溶, 2――用稀硫酸浸溶,
3――冻融后用蒸馏水浸溶,4――曝晒后用蒸馏水浸溶;
3%等――制砖时含铬废渣掺入的比例。
已知我国规定“固体废弃物浸出标准值含铬不得超过10 mg?L-
① 实验取用的砖样符合上述标准;
② 还能得出的其它结论是(写出2条即可) ▲ ; ▲ 。
六、(本题包括1小题,共12分)
19.奶油中含有一种用做香料的有机化合物A,该有机化合物只含有C、H、O三种元素,分子中C、H原子个数比为1:2,其相对分子质量为88,A的结构式中含有碳氧双键。与A相关的反应如下图:
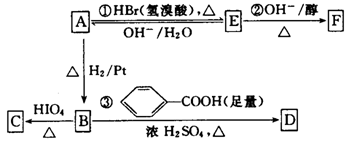
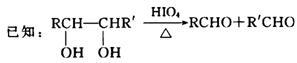
(1)写出反应②的反应类型: ▲ 。
(2)写出A、C、F的结构简式:A ▲ ;C ▲ ;F ▲ 。
(3)请写出同时符合下列条件的A的所有的同分异构体的结构简式:
①链状化合物;②不能与H2发生加成反应;③不能发生银镜反应。
▲ 。
(4)写出反应③的化学方程式: ▲ 。
(5)在空气中长时间搅拌奶油,A可转化为相对分子质量为86的化合物G,G的一氯代物只有一种,写出G的结构简式: ▲ 。
七、(本题包括1小题,共10分)
20.取m g铁粉与含有0.8molHNO3的稀硝酸反应反应后硝酸和铁均无剩余,且硝酸的还原产物只有NO。
(1)若反应后的溶液中滴加KSCN溶液不变红色,则m= ▲ ;
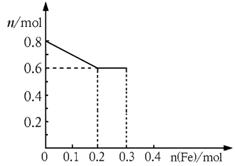 (2)若将铁粉慢慢加入到稀硝酸中,并搅拌,反应过程中溶液里Fe3+、Fe2+、NO3―三种离子中的某离子的物质的量的变化曲线如图所示,则该曲线表示的是_ ▲ _物质的量变化,请你在此图中再画出另外2种离子的物质的量的变化曲线并注明离子种类。
(2)若将铁粉慢慢加入到稀硝酸中,并搅拌,反应过程中溶液里Fe3+、Fe2+、NO3―三种离子中的某离子的物质的量的变化曲线如图所示,则该曲线表示的是_ ▲ _物质的量变化,请你在此图中再画出另外2种离子的物质的量的变化曲线并注明离子种类。
(3)在(2)反应后的溶液中加入含0.1molH2SO4的稀硫酸,计算还能产生的气体的体积(标况下)。
八、(本题包括1小题,共12分)
21.材料(选修三课本第44页实验2-2):向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
(1)写出与H2O分子互为等电子体的微粒 ▲ (填2种)。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是 ▲ 。
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
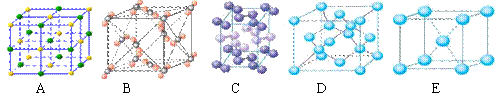
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是 ▲ (请用相应的编号填写)。

Ⅱ.胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上。
(4)写出铜原子价电子层的电子排布式 ▲ ,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有 ▲ (填元素符号)。
(5)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有 ▲ 。
(6)实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4?H2O晶体。实验中所加C2H5OH的作用是 ▲ 。
(西亭中学高三备课组命题 通州教研室审定)
题号
1
2
3
4
5
6
7
8
答案
C
D
B
B
D
C
A
A
题号
9
10
11
12
13
14
答案
CD
AD
C
A
BD
B
15、(本题共10分)
(1)CO32-水解成碱性,Cu2+与OH‑结合生成Cu(OH)2 (合理给分)。 (2分)
(2)取最后一次洗涤液,滴加BaCl2溶液,无沉淀生成,说明已洗净。(2分)
(3)CuSO4、澄清石灰水 (每个1分,名称和化学式搞混不给分,共2分)
(4)B中无水硫酸铜变蓝,澄清石灰水不变浑浊(每点1分,共2分)
(5)装置中原有的空气有影响;实验结束后装置中残留的气体不能被吸收;石灰水可能会吸收空气中的CO2。(2分,说出二点即可)
16、(本题共8分)
(1)腐蚀建筑物、桥梁、工业设备、运输工具;直接破坏农作物、草原、森林;使土壤、湖泊酸化。(说出其中二点即可)(2分)
(2)铁粉和稀硫酸(2分)
(3) 2Fe3+ + SO2 +2 H2O = 2Fe2+ + SO42- + 4H+ (2分)
(4) FeSO4?7H2O (2分)
17、(本题共10分)
(1) A D (每个1分,共2 分,有错不给分)
(2) A
(3) X=2 (2分) , A (2分)
(4) 1/1620(或6.17×10-4) (2分)
18.(10分)
(1)重金属离子会使蛋白质变性(2分)
(2)① Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O (2分)
② Cr3+ + 4OH- = CrO2- + 2H2O (2分)
③ 8~10 (2分)
(3)② (以下任意2条即可)(2分)
其它条件相同时,含铬废渣掺入的比例越大,Cr元素浸出的浓度越高;
酸性环境对Cr元素浸出有抑制作用;
冻融对Cr元素浸出影响不明显;
曝晒对Cr元素浸出影响不明显;
……
19、(共12分)
(1)消去反应 (1分)
(2) 、CH3CHO、
、CH3CHO、 (每空1分,共3分)
(每空1分,共3分)
(3)CH3COOCH2CH3、CH3CH2COOCH3、CH3CH2CH2COOH、(CH3)2CHCOOH
(对一个得1分,错一个倒扣1分,共4分)
(4)CH3CH(OH)CH(OH)CH3 +
(5) (2分)
(2分)
 20.(10分)
20.(10分)
⑴ 16.8 (2分)
⑵NO3―
(每个2分,共6分)
(3)解:3Fe2+ + NO3- + 4H+ = 3Fe3++NO↑+2H2O
0.3mol 0.6mol 0.2mol
Fe2+、NO3-过量,故产生NO气体:0.2mol÷4×
21.(每小题2分,共12分)
(1)H2S、NH2- (2)A (3)BC
(4)3d104s1 Cr (5)共价键、配位键
(6)降低Cu(NH3)4SO4?H2O的溶解度
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com