
题目列表(包括答案和解析)
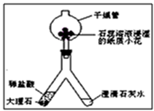 小明对实验室制取二氧化碳的实验进行了相关探究.
小明对实验室制取二氧化碳的实验进行了相关探究.| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
| 吸收液的种类/100mL | 被吸收的CO2体积/mL |
| 蒸馏水 | 82.9 |
| 饱和NaCl溶液 | 58.6 |
| 饱和Na2SO4溶液 | 56 |
| 饱和NaHCO3溶液 | 120 |
| A、4.4克 | B、8.8克 | C、13.2克 | D、17.6克 |
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com