(2013?南京)某兴趣小组对物质的性质进行相关探究、
【提出问题】氯化氢(HCl)气体显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图1的三个实验:
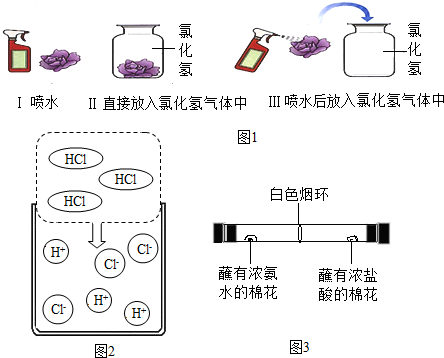
实验现象:Ⅰ和Ⅱ中小花不变色;Ⅲ中小花变红色.
【查阅资料】图2是同学们查阅的氯化氢气体溶于水的示意图.
【实验结论】氯化氢气体不显酸性.
【交流反思】
(1)从微观角度分析氯化氢气体不显酸性的原因是
在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性
在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性
.
(2)小明向实验Ⅲ中变红的小花上喷足量的稀氢氧化钠溶液,发现小花最后变成黄绿色,写出相关反应的化学方程式
NaOH+HCl=NaCl+H2O
NaOH+HCl=NaCl+H2O
.
(3)紫甘蓝的汁液在酸性溶液中显
红
红
色.
(4)下列实验可以用来说明氯化氢气体不显酸性的是
B
B
.
A、测试盐酸的导电性,盐酸能导电
B、干燥的碳酸钠粉末放入氯化氢气体中,不反应
C、氢气与氯气反应,生成氯化氢气体
D、干燥的碳酸钠粉末放入盐酸中,能反应
【拓展应用】
(1)该兴趣小组的同学为探究分子的运动情况,在玻璃管两端同时放入蘸有试剂的棉花,做了如图3所示实验,发现在玻璃管内形成了白色烟环(成分为氯化铵)且偏向蘸有浓盐酸的棉花一端.
①白色烟环偏向蘸有浓盐酸的棉花一端的原因是
氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端
氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端
.
②写出该反应的化学方程式
NH3+HCl=NH4Cl
NH3+HCl=NH4Cl
.
(2)氢气在氯气中燃烧生成氯化氢气体,燃烧100g氢气,理论上生成氯化氢气体的质量是多少?(在答题卡上写出计算过程)



 省略).
省略).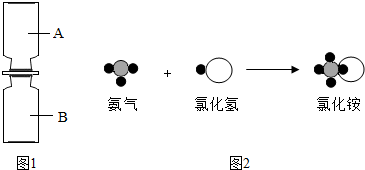 (2012?连云港一模)在化学晚会上,小军同学表演了一个化学小魔术“空瓶生烟”(如图1所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题:若用“
(2012?连云港一模)在化学晚会上,小军同学表演了一个化学小魔术“空瓶生烟”(如图1所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题:若用“ ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用图2表示.
”表示氯原子,上述反应过程可用图2表示.