
题目列表(包括答案和解析)

| A.铝原子中的质子数为13 |
| B.在化合物中铝通常显+3价 |
| C.铝是地壳中含量最多的元素 |
| D.铝可作导线是由于它具有良好的导电性 |

| 实验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加_______ | 有气泡产生 | 固体B含有Cu 、Ag和_ |

| 实验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加______ | 有气泡产生 | 固体B含有Cu、Ag和______ |

金属用途广泛,其结构和性质等是化学的重要研究内容。
 (1)如图是铝的原子结构示意图。下列说法不正确的是_______。
(1)如图是铝的原子结构示意图。下列说法不正确的是_______。
A .铝原子中的质子数为13
.铝原子中的质子数为13
B. 在化合物中铝通常显+3价
在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
 (2)某化学小组用一定量的AgNO3和Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成
(2)某化学小组用一定量的AgNO3和Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成 分进行了分析和研究。
分进行了分析和研究。
【提出问题】溶液A中的溶质可能有哪些?
【做出猜想】
① 只有Zn(NO3)2 ② Zn(NO3)2、AgNO3
③ Zn(NO3)2、Cu(NO3)2 ④ Zn(NO3)2、Cu(NO3)2、AgNO3
【交流讨论】不合理的猜想是_____ __(填标号),其理由是_____ __。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
| 实验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加_______ | 有气泡产生 | 固体B含有Cu 、Ag和_ |
(3)新型材料纳米级 Fe 粉具有广泛的用途,它比普通 Fe 粉更易与氧气反应,其制备工艺流程如图所示:
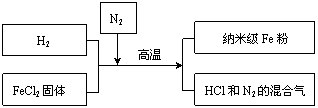
请回答下列问题:
①纳米级Fe粉在空气中易自燃。实验中通入N2 的目的是___ ____。
的目的是___ ____。
②写出H2还原FeCl2,置换出铁的化学方程式___ ____。

汽车是现代生活中不可缺少的代步工具。请回答下列问题:
(1)汽车电路中的导线大都是铜制的,这是利用了金属铜的延展性和____________性。
(2)下列汽车配件及用品中,属于有机合成材料的是(填序号,下同)__________。




a.钢铁外壳 b.玻璃车窗 c.橡胶轮胎 d.羊毛座垫
(3)铁在潮湿的空气中容易锈蚀。
①汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝____________和水。
②喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,有无色气泡逸出,反应的化学方程式是___________;___________。
 (4)回收再利用生锈的铁制品是保护金属资源的一种有效途径。右图所示的废铁粉中Fe2O3含量大约在80%(其余20%为铁)左右,回收后在工业上常用一氧化碳将其还原,反应的化学方程式是_______________,若回收100 t这样的废铁粉可以得到__________t铁。
(4)回收再利用生锈的铁制品是保护金属资源的一种有效途径。右图所示的废铁粉中Fe2O3含量大约在80%(其余20%为铁)左右,回收后在工业上常用一氧化碳将其还原,反应的化学方程式是_______________,若回收100 t这样的废铁粉可以得到__________t铁。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com