
题目列表(包括答案和解析)
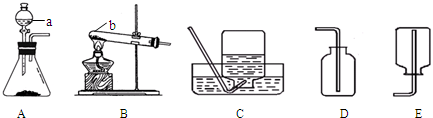
| ||
| ||
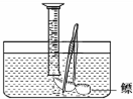
| 方法 | 现象 | 结论 | |
| 验证鳔 内含O2 |
用燃烧的木条检验 用燃烧的木条检验 |
木条能继续燃烧 木条能继续燃烧 |
鳔内含有氧气 鳔内含有氧气 |
| ||
| ||
| ||
| ||
 某化学兴趣小组在老师指导下,进行了“H2O2生成O2的快慢与什么因素有关”的实验.请你帮助回答下列问题.(实验均在20℃室温下进行)
某化学兴趣小组在老师指导下,进行了“H2O2生成O2的快慢与什么因素有关”的实验.请你帮助回答下列问题.(实验均在20℃室温下进行)
| ||
| ||
| 实验编号 | 1 | 2 |
| 反应物 | 6% H2O2 | 6% H2O2 |
| 催化剂 | 1g红砖粉 | 1g MnO2 |
| 时间(s) | 152 | 35 |
| 实验编号 | 1 | 2 | 3 |
| H2O2溶液的溶质质量分数 | 5% | 10% | 20% |
| MnO2粉末用量(g) | 0.2 | ||
| 收集到500mL气体时所用时间(s) | 205 | 80 | 9 |
| 反应后溶液的温度(℃) | 39 | 56 | 67 |
某化学课外活动小组进行了一系列的实验,请按要求作答:
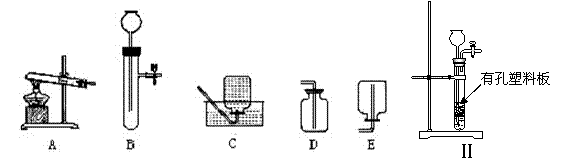
(1)按要求从以上A — E装置中选择(填装置的序号)。小镁同学要用高锰酸钾加热制取并收集O2应选择 装置,反应的化学方程式为 ; B装置也可用于制取O2,反应的化学方程式为 ;
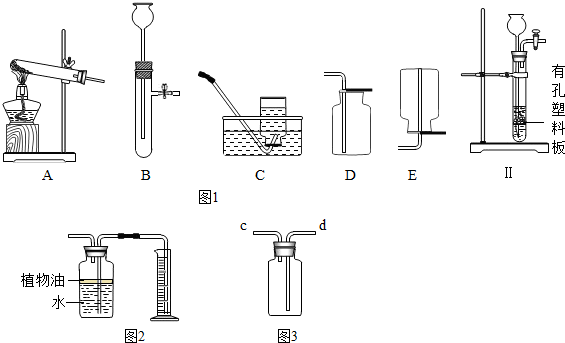
(2) 小松同学改进B装置后,设计出如图(Ⅱ)装置,此装置的优点是: ;
(3)小松同学使用图(Ⅱ)装置制取CO2,现有①粉末状石灰石;②块状大理石;③稀HCl;④稀H2SO4四种试剂,应选用的试剂是 (填序号)。
(3) 验证二氧化碳气体己收集满的方法是______________________________
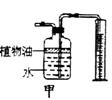
(4) 甲图装置可用来测量生成的C02气体的体积,其中在水面上放一层植物油的目的是_______________,植物油上方原有的空气对实验的结果 (填“有”或“没有”)明显影响。
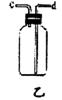
(5) 氨气(NH3)在通常状况下是一种无色有强烈刺激性气味的气体,密度比空气小,极易溶于水,其水溶液为氨水。实验室可用加热氯化铵和熟石灰两种固体混合物的方法制取氨气。实验室制取氨气应选用的发生装置是_______(填字母),若用乙图装置收集氨气,气体应从______端导气管进入瓶 中
中
(填字母)。
(6) 根据上述分析和选择可知,实验室制取气体选择发生装置的依据是 。若用排空气法收集气体,导气管应伸入 集气瓶底部,否则 ;小明同学建议用装置B做“H202分解制取02”实验,但遭到很多同学的质疑,你认为用该装置制取02的缺点是 ,小红将仪器作一简单的调整即得到目的,小红的做法是 。
集气瓶底部,否则 ;小明同学建议用装置B做“H202分解制取02”实验,但遭到很多同学的质疑,你认为用该装置制取02的缺点是 ,小红将仪器作一简单的调整即得到目的,小红的做法是 。
 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com