
题目列表(包括答案和解析)
| 物 质 | MgO | MgCl2 | Mg2N3 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |

| 反应前镁带的质量 | 反应的固体产物的质量 | |
| 第一次 | 2.4046g | 3.8854g |
| 第二次 | 2.4024g | 3.8839g |
| 第三次 | 2.4063g | 3.8857g |
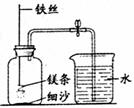
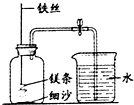 某校研究性学习小组用右图装置(气密性良好)进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.
某校研究性学习小组用右图装置(气密性良好)进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.| 物 质 | MgO | MgCl2 | Mg2N3 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
| 反应前镁带的质量 | 反应的固体产物的质量 | |
| 第一次 | 2.4046g | 3.8854g |
| 第二次 | 2.4024g | 3.8839g |
| 第三次 | 2.4063g | 3.8857g |
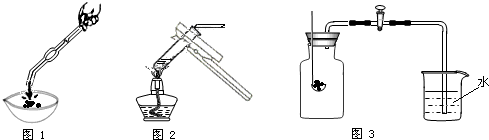
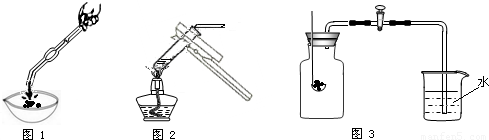
 某校研究性学习小组用右图装置(气密性良好)进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%。
某校研究性学习小组用右图装置(气密性良好)进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%。
【分析】根据空气中氧气的体积分数,如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积约占其容积的 %。现进入集气瓶中水的体积约为其容积的70%,所以减少的气体中有氮气。
【提出问题】氮气是怎样减少的呢?
【猜想与假设】(1)氮气与镁条反应而减少;(2) 。
【查阅资料】镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体。氮化镁中氮元素的化合价为 ;镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁。
【结论】氮气减少是由于镁与氮气发生了反应。
【反思与拓展】(1)镁带充分燃烧后,集气瓶中剩余的气体主要是 。
(2)通过以上探究,你对燃烧的有关知识有了什么新的认识:
(写出一点即可)。
(3)用燃烧法测定空气中氧气含量时,对药品的要求是 。
| 物 质 | MgO | MgCl2 | Mg2N3 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
| 反应前镁带的质量 | 反应的固体产物的质量 | |
| 第一次 | 2.4046g | 3.8854g |
| 第二次 | 2.4024g | 3.8839g |
| 第三次 | 2.4063g | 3.8857g |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com