
ЈЁ2013?ОчіЗЗш¶юДЈЈ©ОТ№ъ№Еҙъ·ДЦҜТөіЈҪ«ІЭДҫ»ТЈЁЦчТӘіЙ·ЦK
2CO
3Ј©әНЙъКҜ»ТФЪЛ®ЦР»мәПЈ¬УГЙПІгЗеТәЖҜ°ЧЦҜОпЈ®
CaЈЁOHЈ©
2Ј¬K
2CO
3әНKOHөДІҝ·ЦИЬҪв¶ИИзПВұн
ЎҫЧКБПЎҝўЩK
2CO
3+CaЈЁOHЈ©
2ЁTCaCO
3Ўэ+2KOH
ўЪCaЈЁOHЈ©
2Ј¬K
2CO
3әНKOHөДІҝ·ЦИЬҪв¶ИИзПВұнЈ®
| ОВ¶И/Ўж |
0 |
10 |
20 |
30 |
50 |
| ИЬҪв¶И/g |
CaЈЁOHЈ©2 |
0.18 |
0.17 |
0.16 |
0.15 |
0.14 |
| k2CO3 |
107 |
109 |
110 |
114 |
121 |
| KOH |
97 |
103 |
112 |
126 |
140 |
ЈЁ1Ј©20ЎжКұЈ¬100gЛ®ЦРЧо¶аҝЙИЬҪвK
2CO
3өДЦКБҝКЗ
110
110
gЈ®ИЬЦКөДЦКБҝ·ЦКэОӘ50%өДKOHИЬТәКфУЪ
І»ұҘәН
І»ұҘәН
ИЬТәЈЁМоЎ°ұҘәНЎұ»тЎ°І»ұҘәНЎұЈ©
ЈЁ2Ј©ДіОВ¶ИКұЈ¬ПтТ»¶ЁБҝөДұҘәНЗвСх»ҜёЖИЬТәЦРјУИлЙЩБҝЙъКҜ»ТЈ¬»ЦёҙөҪФӯОВ¶ИЈ¬ДіР©БҝЛжКұјдұд»ҜөД№ШПөИзНјЛщКҫЈ®ФтЧЭЧшұкҝЙДЬұнКҫөДКЗ
ac
ac
ЈЁМоРтәЕЈ©
aЈ®ИЬЦКөДЦКБҝ bЈ®ИЬјБөДЦКБҝ cЈ®ИЬТәөДЦКБҝ dЈ®ИЬЦКөДЦКБҝ·ЦКэ eЈ®ЗвСх»ҜёЖөДИЬҪв¶ИЈ®
ЈЁ3Ј©20ЎжКұЈ¬Ҫ«1.38gK
2CO
3№ММе·ЕИл100gЛ®ЦРЈ¬ІўјУИлТ»¶ЁБҝөДЗвСх»ҜёЖЈ¬ҪБ°иК№Ждід·Ц·ҙУҰЈ¬»ЦёҙөҪФӯОВ¶ИЈ¬№эВЛЈ¬өГөҪЦКБҝОӘ1.1gөД№ММеЈ®ЛщөГВЛТәЦРөДИЬЦККЗ
ЗвСх»ҜјШәНЗвСх»ҜёЖ
ЗвСх»ҜјШәНЗвСх»ҜёЖ
Ј¬ЙъіЙМјЛбёЖөДЦКБҝКЗ
1
1
gЈ®

 ЈЁ2013?ОчіЗЗш¶юДЈЈ©ОТ№ъ№Еҙъ·ДЦҜТөіЈҪ«ІЭДҫ»ТЈЁЦчТӘіЙ·ЦK2CO3Ј©әНЙъКҜ»ТФЪЛ®ЦР»мәПЈ¬УГЙПІгЗеТәЖҜ°ЧЦҜОпЈ®
ЈЁ2013?ОчіЗЗш¶юДЈЈ©ОТ№ъ№Еҙъ·ДЦҜТөіЈҪ«ІЭДҫ»ТЈЁЦчТӘіЙ·ЦK2CO3Ј©әНЙъКҜ»ТФЪЛ®ЦР»мәПЈ¬УГЙПІгЗеТәЖҜ°ЧЦҜОпЈ®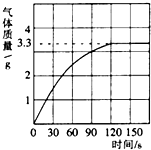 ДіРЈ»ҜС§РЛИӨРЎЧйН¬С§ҪшРРДіҙуАнКҜЦРМјЛбёЖә¬БҝөДІв¶ЁКөСйЈ¬ИЎ12.5gҙуАнКҜСщЖ·УлЧгБҝөДПЎСОЛбід·Ц·ҙУҰЈ¬ІъЙъCO2ЖшМеөДЗйҝцИзНјЛщКҫЈ®
ДіРЈ»ҜС§РЛИӨРЎЧйН¬С§ҪшРРДіҙуАнКҜЦРМјЛбёЖә¬БҝөДІв¶ЁКөСйЈ¬ИЎ12.5gҙуАнКҜСщЖ·УлЧгБҝөДПЎСОЛбід·Ц·ҙУҰЈ¬ІъЙъCO2ЖшМеөДЗйҝцИзНјЛщКҫЈ®