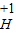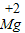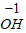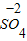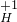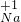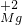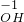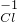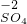小明学习了金属的活动顺序后,到实验室进行探究,他将一块金属钠投入到硫酸铜溶液中想得到铜,但却看到了另外的现象:没有红色的物质析出,却生成了大量的气体,并出现了蓝色的沉淀.小明想到了硫酸铜溶液中有水,又补充了另一个实验.并记录如下:
| 操作步骤 |
实验现象 |
| ①将一小块钠放入盛水的烧杯中 |
金属溶解,剧烈反应,产生大量气体 |
| ②相反应后的烧杯中滴加酚酞试液 |
酚酞试液变红色 |
| ③将产生的气体收集并点燃 |
该气体能燃烧,并产生淡蓝色火焰 |
【分析】由上述现象可知:金属钠
能
能
(填“能”或“不能”)与水反应,生成物中呈碱性的物质此处是
NaOH
NaOH
(填“NaOH”或“Na
2CO
3”),其理由是
化学反应前后元素的种类不变,而水中不含碳元素
化学反应前后元素的种类不变,而水中不含碳元素
.其反应的化学方程式为
2Na+2H2O=2NaOH+H2↑
2Na+2H2O=2NaOH+H2↑
.
【结论】据上述现象,小明又写出了金属钠投入到硫酸铜溶液中另一个产生沉淀的反应化学方程式
2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
.
【反思】在金属活动顺序里,位于前面的金属不一定能把后面的金属从其他化合物的溶液中置换出来.
【拓展】将金属钠在空气中点燃后再放入充满CO
2的集气瓶中,发现钠继续剧烈燃烧,发出白光,放热,产生一种白色固体和一种黑色固体.已知该反应为置换反应,发生的方程式为
.这个实验使你对燃烧条件产生的新认识是
燃烧不一定需要氧气
燃烧不一定需要氧气
.

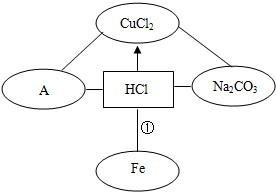 右图是关于盐酸化学性质的知识网络,-”表示相连的两种物质能发生反应,“”表示一种物质转化成另一种物
右图是关于盐酸化学性质的知识网络,-”表示相连的两种物质能发生反应,“”表示一种物质转化成另一种物