有两个实验小组同学为探究过氧化钠与二氧化碳的反应,用如图所示的装置进行实验.通入CO
2气体,将带余烬的木条插入试管C

中,木条复燃.
请回答下列问题:
(1)第一小组同学认为Na
2O
2与CO
2反应生成了碳酸钠和氧气,该反应的化学方程式是
2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2CO2═2Na2CO3+O2
.
(2)请设计一种实验方案,证明过氧化钠与二氧化碳反应生成白色固体中含有碳酸钠,
取反应后生成的固体,加稀盐酸,生成使澄清石灰水变浑浊的气体(或取反应后生成的固体,加CaCl2溶液,生成白色沉淀或其他合理答案)
取反应后生成的固体,加稀盐酸,生成使澄清石灰水变浑浊的气体(或取反应后生成的固体,加CaCl2溶液,生成白色沉淀或其他合理答案)
.
(3)第二小组同学认为Na
2O
2与CO
2反应除了生成碳酸钠和氧气外,还有氢氧化钠和硫酸钠生成,请你从化学反应的实质上说出你同意或不同意他们的理由
不同意.根据质量守恒定律,化学反应前后原子的种类不变,反应物的分子中没有氢原子,故不可能生成NaHCO3
不同意.根据质量守恒定律,化学反应前后原子的种类不变,反应物的分子中没有氢原子,故不可能生成NaHCO3
.


 中,木条复燃.
中,木条复燃.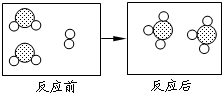 18、下图形象地表示了在高温、催化剂条件下,某化学反应前后反应物与生成物分子及其数目的变化,其中
18、下图形象地表示了在高温、催化剂条件下,某化学反应前后反应物与生成物分子及其数目的变化,其中 表示硫原子,
表示硫原子, 表示氧原子.
表示氧原子. 甲、乙、丙、丁、X都是初中化学常见的物质,它们之间的关系如下图所示.(图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系;部分反应物、生成物及反应条件均已略去.)(1)若上述物质由C、O、Fe三种元素中的一种或几种组成.
甲、乙、丙、丁、X都是初中化学常见的物质,它们之间的关系如下图所示.(图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系;部分反应物、生成物及反应条件均已略去.)(1)若上述物质由C、O、Fe三种元素中的一种或几种组成.