
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
œ÷”– ß»•±Í«©µƒ5÷÷ŒÞ…´»Ð“∫£¨∑÷± «Na2CO3°¢NaCl°¢Ca£®OH£©2°¢NaOH∫Õœ°—ŒÀ·£¨»Œ»°∆‰÷–µƒ4÷÷Ã˘…œA°¢B°¢C°¢D±Í«©£¨Ω¯––»Áœ¬ µ—È£Æ
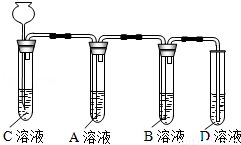
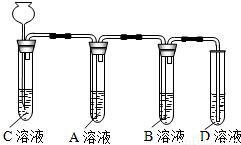
£®1£©“¿æð»ÁÕº◊∞÷√Ω¯–– µ—È£¨∆‰÷–º–≥÷πÃ∂®◊∞÷√“—¬‘»•£Æ¥”≥§æ±¬©∂∑º”»Îœ°—ŒÀ·£¨ø…“‘π€≤ϵΩC»Ð“∫÷–”–∆¯≈ð≤˙…˙£¨A»Ð“∫÷–”–∞◊…´≥¡µÌ…˙≥…£¨B°¢D»Ð“∫æ˘ŒÞ√˜œ‘±‰ªØ£Æ‘ÚC»Ð“∫”Îœ°—ŒÀ·∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™ £ªA»Ð“∫÷–∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™ £Æ
£®2£©»°…Ÿ¡øB»Ð“∫µπ»Î’Ù∑¢√Û£¨º”»»£¨Œ≈µΩ”–¥Ãº§–‘∆¯Œ∂£¨Õ£÷πº”»»£Æ‘Ÿ»°…Ÿ¡øD»Ð“∫µπ»Î¡Ì“ª’Ù∑¢√Û£¨º”»»£¨”–∞◊…´πÃÃÂŒˆ≥ˆ£¨Õ£÷πº”»»£Æ‘ÚB « £Æ
£®3£©Õ¨—ß√«»œŒ™ µ—È£®1£©∑¥”¶∫ÛµƒD»Ð“∫÷–»Ð÷ µƒ≥…∑÷”–∂ý÷÷ø…ƒÐ£¨«Îƒ„…˺∆ µ—È∑Ω∞∏÷§√˜ °£ 
œ÷”– ß»•±Í«©µƒ5÷÷ŒÞ…´»Ð“∫£¨∑÷± «Na2CO3°¢NaCl°¢Ca£®OH£©2°¢NaOH∫Õœ°—ŒÀ·£¨»Œ»°∆‰÷–µƒ4÷÷Ã˘…œA°¢B°¢C°¢D±Í«©£¨Ω¯––»Áœ¬ µ—È£Æ
£®1£©“¿æð»ÁÕº◊∞÷√Ω¯–– µ—È£¨∆‰÷–º–≥÷πÃ∂®◊∞÷√“—¬‘»•£Æ¥”≥§æ±¬©∂∑º”»Îœ°—ŒÀ·£¨ø…“‘π€≤ϵΩC»Ð“∫÷–”–∆¯≈ð≤˙…˙£¨A»Ð“∫÷–”–∞◊…´≥¡µÌ…˙≥…£¨B°¢D»Ð“∫æ˘ŒÞ√˜œ‘±‰ªØ£Æ‘ÚC»Ð“∫”Îœ°—ŒÀ·∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™ £ªA»Ð“∫÷–∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™ £Æ
£®2£©»°…Ÿ¡øB»Ð“∫µπ»Î’Ù∑¢√Û£¨º”»»£¨Œ≈µΩ”–¥Ãº§–‘∆¯Œ∂£¨Õ£÷πº”»»£Æ‘Ÿ»°…Ÿ¡øD»Ð“∫µπ»Î¡Ì“ª’Ù∑¢√Û£¨º”»»£¨”–∞◊…´πÃÃÂŒˆ≥ˆ£¨Õ£÷πº”»»£Æ‘ÚB « £Æ
£®3£©Õ¨—ß√«»œŒ™ µ—È£®1£©∑¥”¶∫ÛµƒD»Ð“∫÷–»Ð÷ µƒ≥…∑÷”–∂ý÷÷ø…ƒÐ£¨«Îƒ„…˺∆ µ—È∑Ω∞∏÷§√˜ °£

ƒ≥Õ¨—ß¿˚”√ªØπ§≥ßµƒ∑œºÓ“∫(÷˜“™≥…∑÷Œ™Na2CO3£¨ªπ∫¨”–…Ÿ¡øNaCl£¨∆‰À¸‘”÷ ≤ªº∆)∫Õ Øª“»ÈŒ™‘≠¡œ÷∆±∏…’ºÓ£¨≤¢∂‘À˘µ√µƒ…’ºÓ¥÷≤˙∆∑µƒ≥…∑÷Ω¯––∑÷Œˆ∫Õ≤‚∂®£Æ
[¥÷≤˙∆∑÷∆±∏](1)Ω´∑œºÓ“∫º”»»’Ù∑¢≈®Àı£¨–Œ≥…Ωœ≈®µƒ»Ð“∫£¨¿‰»¥∫۔Πت“»ÈªÏ∫œ£¨∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™________£Æ
(2)Ω´∑¥”¶∫ÛµƒªÏ∫œŒÔπ˝¬À£¨µ√µΩµƒ¬À“∫Ω¯––’Ù∑¢Ω·æߣ¨÷∆µ√NaOH¥÷≤˙∆∑£Æ
[¥÷≤˙∆∑≥…∑÷∑÷Œˆ](1)»° ¡ø¥÷≤˙∆∑»Ð”⁄ÀÆ£¨µŒº”Ba(NO3)2»Ð“∫≥ˆœ÷∞◊…´ªÎ◊«£¨∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™________£¨∏√¥÷≤˙∆∑÷–“ª∂®≤ª∫¨”–________£¨¿Ì”… «________£Æ
(2)∏√–°◊ÈÕ¨—ßÕ®π˝∂‘¥÷≤˙∆∑≥…∑÷µƒ µ—È∑÷Œˆ£¨»∑∂®∏√¥÷≤˙∆∑÷–∫¨”–»˝÷÷ŒÔ÷ £Æ
[¥÷≤˙∆∑∫¨¡ø≤‚∂®]Na2CO3∫¨¡øµƒ≤‚∂®£∫
(1)∏√–À»§–°◊ȵƒÕ¨—߅˺∆¡Àœ¬ÕºÀ˘ 浃 µ—È◊∞÷√£Æ»°10.0 g¥÷≤˙∆∑£¨Ω¯–– µ—È£Æ
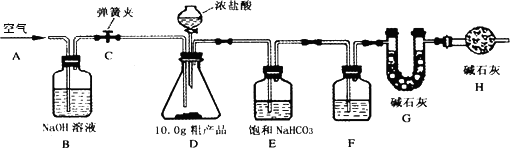
[Àµ√˜]ºÓ ت“ «CaO”ÎNaOHµƒπÃêÏ∫œŒÔ£ÆE◊∞÷√÷–µƒ±•∫ÕNaHCO3»Ð“∫ «Œ™¡À≥˝»•∂˛—ıªØú∆¯ÃÂ÷–µƒ¬»ªØ«‚£¨∑¢…˙µƒ∑¥”¶Œ™NaHCO3£´HC1£ΩNaCl ÆCO2°¸ ÆH2O£Æ
(2)≤Ÿ◊˜≤Ω÷Ë
¢Ÿ¡¨Ω”∫√◊∞÷√£¨ºÏ≤È∆¯√Ж‘£ª¢⁄¥Úø™µØª…º–C£¨‘⁄A¥¶ª∫ª∫Õ®»Î“ª∂Œ ±º‰ø’∆¯£ª¢€≥∆¡øGµƒ÷ ¡ø£ª¢Ðπÿ±’µØª…º–C£¨¬˝¬˝µŒº”≈®—ŒÀ·÷¡π˝¡ø£¨÷±÷¡D÷–ŒÞ∆¯≈ð√∞≥ˆ£ª¢ð¥Úø™µØª…º–C£¨‘Ÿ¥Œª∫ª∫Õ®»Î“ª∂Œ ±º‰ø’∆¯£ª¢Þ‘Ÿ¥Œ≥∆¡øGµƒ÷ ¡ø£¨µ√«∞∫Û¡Ω¥Œ÷ ¡ø≤ÓŒ™0.48 g£Æ
(3)Œ ÂÃΩæø°°F÷–µƒ ‘º¡”¶Œ™________£¨B◊∞÷√µƒ◊˜”√ «________£¨H◊∞÷√µƒ◊˜”√ «________£Æ
»Ù√ª”–H◊∞÷√£¨‘Ú≤‚∂®µƒNa2CO3µƒ÷ ¡ø∑÷ ˝ª·________(ÃÓ°∞∆´¥Û°±°¢°∞∆´–°°±°¢°∞≤ª±‰°±)£Æ ¬ µ…œ10.0 g¥÷≤˙∆∑÷ªƒÐ≤˙…˙0.44 g°°CO2£Æ«Îƒ„◊–œ∏∑÷Œˆ…œ ˆ µ—È£¨Ω‚ Õ µ—È÷µ0.48 g±»’˝»∑÷µ0.44 g∆´¥Ûµƒ‘≠“Ú(ºŸ…Ë≤Ÿ◊˜æ˘’˝»∑)________
(4) ˝æðº∆À„
∏˘æð’˝»∑÷µ0.44 gø…«Ûµ√¥÷≤˙∆∑÷–Na2CO3µƒ÷ ¡ø∑÷ ˝Œ™________£•£Æ
NaOH∫¨¡øµƒ≤‚∂®£∫∏√–°◊ÈÕ¨—ß”÷¡Ì»°10.0 g¥÷≤˙∆∑£¨÷µŒº”»Î20£•µƒ—ŒÀ·÷¡«°∫√ÕÍ»´∑¥”¶ ±£¨œ˚∫ƒ—ŒÀ·µƒ÷ ¡øŒ™36.5 g£Æ∑≈≥ˆCO2°°0.44 g(≤ªøº¬«∂˛—ıªØú∆¯Ãµƒ»ÐΩ‚)£Æ«Û‘≠¥÷≤˙∆∑÷–NaOHµƒ÷ ¡ø∑÷ ˝£Æ(–¥≥ˆº∆À„π˝≥Ã)
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com