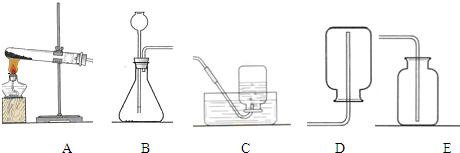
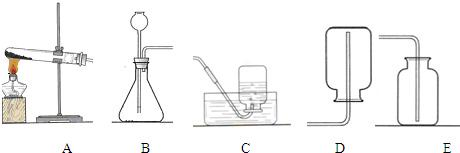
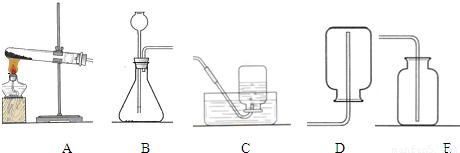
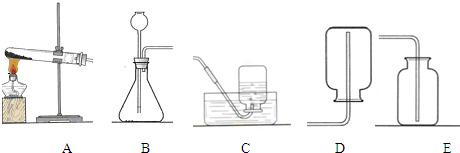
(2013?长宁区一模)某化学兴趣小组的同学按照课本实验方法(如图甲),做木炭与氧化铜反应的实验时,发现很难观察到有亮红色金属铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进.

【提出问题】暗红色的固体是什么?如何选择合适的条件,使木炭还原氧化铜的实验现象更明显?
【查阅资料】铜元素有+1和+2两种化合价,氧元素的化合价通常为-2.
【猜想与假设】
(1)同学们认为这种暗红色固体可能是另一种铜元素的氧化物,并猜测它的化学式为
Cu2O
Cu2O
.
(2)同学们还认为,通过改变反应物的状态、质量比,以及反应装置等,可以使该实验现象更加明显,减少出现暗红色固体的情况.
【分析与交流】
(1)小赟建议用超细炭粉与氧化铜粉末充分混合高温加热进行实验.你认为这样建议的原因是
增大反应物接触面积,使反应更充分
增大反应物接触面积,使反应更充分
,该反应的化学方程式为
.
(2)小慧认为稳定的高温是本实验成功的关键因素之一,建议在酒精灯火焰处加金属网罩(如图乙),使酒精灯外焰完全包围试管的下部,其作用是
集中火焰,提高温度
集中火焰,提高温度
.
【实验与结论】
同学们决定按改进后的方案进行实验.他们在检查了乙装置的
气密性
气密性
后,往试管中加入已充分干燥的超细炭粉与氧化铜粉末的混合物,并开始加热,当看到澄清的石灰水刚刚有稍许浑浊时,
不能
不能
(填“可以”或“不能”)确定氧化铜和炭粉已经开始反应.待反应结束,先将导气管从石灰水中取出,然后立即关闭止水夹,让产物自然冷却.若不及时关闭止水夹,可能出现的问题是
生成的铜再次被氧化
生成的铜再次被氧化
.待产物冷却后,同学们终于看到了期待已久的亮红色金属铜,实验获得了圆满成功.