
题目列表(包括答案和解析)
| ||
| ||
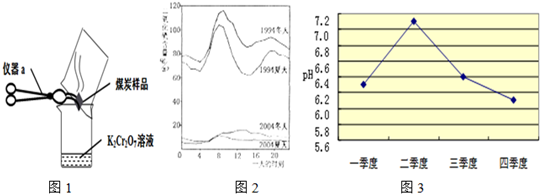
 +H2O”.然而化学方程式中有一生成物不清楚,请根据已学知识推测其化学式:
+H2O”.然而化学方程式中有一生成物不清楚,请根据已学知识推测其化学式:| 测定时间/分钟 | 0 | 1 | 2 | 3 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容. D.碳的相对原子质量为12.01
D.碳的相对原子质量为12.01
| ||
| 叶绿体 |
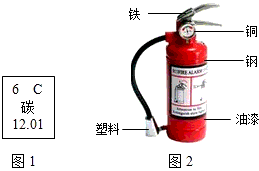 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.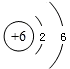 D.碳的相对原子质量为12.01
D.碳的相对原子质量为12.01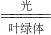 C6H12O6+6O2,则X的化学式为________.
C6H12O6+6O2,则X的化学式为________.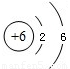 D.碳的相对原子质量为12.01
D.碳的相对原子质量为12.01 C6H12O6+6O2,则X的化学式为 .
C6H12O6+6O2,则X的化学式为 .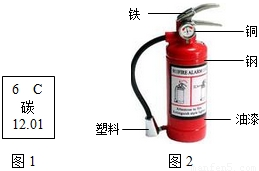
随着经济的发展,环境成为是人们日益关注的问题。
(1)为了降低大气中二氧化碳的含量,化学家们正想尽办法用化学反应的手段使二氧化碳“变废为宝”。用三甲基膦做催化剂,在高压、极低温度条件下,CO2和H2可以高效合成甲酸(HCOOH),并实现了工业化生产。该反应的化学方程式为____________。
(2)目前使用膜分离法从空![]() 气中分离出CO2,这个过程中CO2发生了________ (填“物理”或“化学”)变化。
气中分离出CO2,这个过程中CO2发生了________ (填“物理”或“化学”)变化。
(3)2011年3月,日本福岛第一核电站发生核辐射泄漏。堆芯熔毁是核电事故中最严重的事态。福田第一核电站机组反应堆芯放出氢气,当接触外界的氧气发生剧烈反应,导致连续爆炸。请写出氢气爆炸时的化学方程式__________。
(4)当空气受SO2严重污染时,可通过飞机喷洒X粉末,使空气中的SO2含量明显降低,该过程发生的反应是2X+2SO2+O2 2CaSO4+2CO2。X的化学式是__________。
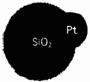 (5)纳米球异质二聚体是纳米自动化产业中的一种新模型(如图所示),它可望用于河流和溪水的污染控制。不溶于水的二氧化硅晶体可以制成微小的纳米球。在铂的催化作用下,双氧水分解,同时使一个二氧化硅纳米球与一个铂纳米球相结合。根据以上信息判断,下列有关说法错误的是__________。
(5)纳米球异质二聚体是纳米自动化产业中的一种新模型(如图所示),它可望用于河流和溪水的污染控制。不溶于水的二氧化硅晶体可以制成微小的纳米球。在铂的催化作用下,双氧水分解,同时使一个二氧化硅纳米球与一个铂纳米球相结合。根据以上信息判断,下列有关说法错误的是__________。
A.二氧化硅纳米球中含有的硅、氧原子个数比为1:2
B.纳米球异质二聚体,其微粒大小在纳米级范围
C.双氧水分解时,二氧化硅是催化剂
D.因为二氧化硅晶体能与水反应而溶解,所以该纳米![]() 级发动机可以用于水污染的控制
级发动机可以用于水污染的控制
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com