纯碱(Na
2CO
3)产品中常含有少量氯化钠.某厂生产的纯碱包装袋上标有“Na
2CO
3含量≧95%”字样.为判断该产品中Na
2CO
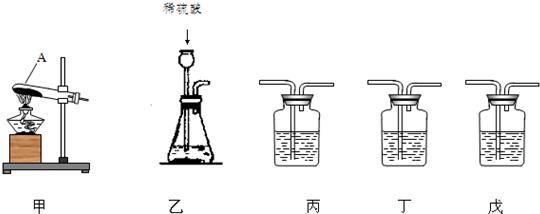
3的含量是否达到要求,称取5.0g样品进行检验,可供选取的装置如下图.其中,丙装置中装足量浓氢氧化钠溶液,丁装置中装浓硫酸,戊装置中装水.(提示:浓硫酸具有吸水性,不挥发,不与二氧化碳反应,碳酸钠受热不分解.)
(1)写出上图仪器A的一种常见用途
用作少量试剂的反应容器.
用作少量试剂的反应容器.
(2)你选择的实验装置从左到右组装排列为(填编号)
乙、丁、丙
乙、丁、丙
.请说出你选择或排列装置的一点理由
由于是固体碳酸与液体稀硫酸反应,所以应选乙装置.
由于是固体碳酸与液体稀硫酸反应,所以应选乙装置.
.
(3)假设每步都反应完全,生成的二氧化碳全部被吸收,不考虑空气中二氧化碳的影响.要较准确地计算“Na
2CO
3含量≧95%”是否真实,该实验除称取样品质量外,还要用天平称量得到的实验数据是
实验前后丙装置的质量
实验前后丙装置的质量
(4)若乙装置中加入浓盐酸(有挥发性),对测量结果有影响.原因是浓盐酸挥发出的氯化氢气体
随二氧化碳气体一起进入丙装置,跟氢氧化钠反应使得到的实验数据不准确.
随二氧化碳气体一起进入丙装置,跟氢氧化钠反应使得到的实验数据不准确.
(5)若实验装置连接正确,实验过程中看到丙装置出现的气泡比丁少得多,一种可能的原因是
丁装置可能漏气
丁装置可能漏气