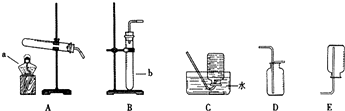
(I)请结合下图所示实验装置回答有关问题:
(1)写出一个实验室制取氧气的化学方程式
,根据该反应原理,可选择图中装置
BD
BD
(填字母编号)制取较干燥的氧气.
(2)实验室制取二氧化碳的化学方程式为
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.你所组装的上述制取氧气的装置
能
能
(填“能”或“不能”)用于实验室制取二氧化碳,理由是
固体与液体反应无需加热与该装置适用范围相同
固体与液体反应无需加热与该装置适用范围相同
.
(II)高芬同学为了比较铁和银的活泼性大小,从实验室找到一生锈的铁钉、一瓶稀硫酸溶液和一瓶硝酸银溶液,郭春杰同学建议她先用硫酸把铁钉上的锈除尽,硫酸能除锈的理由是
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
(填化学方程式),高芬同学用硫酸把铁钉浸泡一段时间发现有气泡产生,产生气泡的原因是
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
(填化学方程式),铁锈除尽后,高芬同学将铁钉洗净、擦干后投入到一定量的硝酸银溶液中发现溶液由无色变成了浅绿色,通过分析她得出:此实验反应的化学方程式为
Fe+2AgNO3=Fe(NO3)2+2Ag
Fe+2AgNO3=Fe(NO3)2+2Ag
,且金属的活泼性是Fe>Ag.反应一段时间后取出铁钉,铁钉变成了银白色的,高芬同学欣喜的说:我得到纯银啦!郭春杰同学经过分析认为剩余的金属有两种可能:①可能是
Fe与Ag混合物
Fe与Ag混合物
;②可能是
Ag
Ag
.请你设计一种方案证明哪种猜想正确
将铁钉碾碎投入到稀硫酸中,观察有无气泡产生,若有气泡则①正确,若无气泡则②正确
将铁钉碾碎投入到稀硫酸中,观察有无气泡产生,若有气泡则①正确,若无气泡则②正确
.

 (I)请结合下图所示实验装置回答有关问题:
(I)请结合下图所示实验装置回答有关问题: