
题目列表(包括答案和解析)
“过 氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气。实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分及其质量。
氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气。实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分及其质量。
 【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【查阅资料】
①2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2═2Na2CO3+O2
②碳酸钠溶液显碱性,氯化钙溶液显中性。
③Na2CO3+ CaCl2═CaCO3↓+2 NaCl
【猜想与假设】
(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是______________ __________的混合物
__________的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
……
【设计实施方案】
| 实验步骤 | 实验现象 |
| ①取3.00g变质粉末于一支大试管内,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体。 | 固体完全溶解,______________________ |
| ②继续向上述试管中加入足量的石灰水,充分反应。 | __________________________________ |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g。 |
【解释与结论】同学们经过认真分析,得出了以下结论。
粉末中含有的成分及质量
| Na2O2 | NaOH | Na2CO3 | |
| 成分(填“有”或“没有”) | |||
| 质量(g) |
【反思与评价】
(1)实验室在保存过氧化钠时应注意_______________。
(2)有同学提出把第②步实验中足量的石灰水改为足量氯化钙溶液,至沉淀不再生成时过滤,向滤液中滴加无色酚酞试液,若液体变红,则证明原粉末中有NaOH。你认为该方案是否合理并说明理由____________________________。
二氧化硫是形成酸雨的罪魁祸首之一。化学小组的同学想对二氧化硫进行研究,依据化学方程式Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O计算后。取一定量的锌粉与98%的浓硫酸恰好完全反应。
ZnSO4+SO2↑+2H2O计算后。取一定量的锌粉与98%的浓硫酸恰好完全反应。
提出问题:对于制得的气体,有同学认为可能含有杂质。
猜想与假设:化学小组制得的SO2中混有的杂质主要是H2。产生这一结果的主要原因是 (用化学方程式和必要的文字说明)。
查阅资料:(1)CO2能与水、 反应,SO2与CO2一样,也能。
(2)H2与CO一样,能将金属氧化物冶炼成金属。
(3)CaSO3难溶于水
实验验证:为证实相关分析,化学小组的同学设计了下图所示装置进行实验。 
(1)B装置的作用是 。
(2)混合气体中含有氢气,则E装置中观察到的现象是 ,反应的化学方程式为 。
实验反思:小芳认为,利用上述装置可以测定混合气体中二氧化硫和氢气的质量比,要达到这一目的,实验小组必须测定下列数据中的 (填字母)。
| A.参加反应的锌的质量 | B.装置B的质量增量 |
| C.氧化铜的质量 | D.装置 F的质量增量 |
过氧化钠(Na2O2)是一种淡黄色固体。在一次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入了如图1的实验装置中,当倾倒二氧化碳时,发现了 现象;同时也惊奇地发现棉花团燃烧了起来。
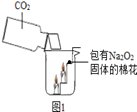
【提出问题】棉花团为什么会燃烧起来呢?
【查阅资料】
(1)在常温下Na2O2能和CO2反应生成一种气体和碱性物质。
(2)在常温下Na2O2能和水发生反应: 2Na2O2+2H2O═4NaOH+O2↑
(3)无水硫酸铜为白色固体,吸水后变为蓝色。
【设计实验】经过讨论后,小组同学设计了如图2的实验进行探究。
【实验步骤】
①检查整套装置的气密性;
②把相关的试剂放入对应的仪器内(D装置的U型管内放有足量的Na2O2固体,烧杯内盛有饱和的澄清石灰水),并按图2组装整套实验仪器;
③用力推动针筒的活塞,把稀盐酸注入试管内;
④一段时间后,在P处放置一根带火星的小木条,观察现象。
注:整个实验中不考虑稀盐酸的挥发和空气对实验的影响。
【实验现象】
①无水硫酸铜 ;②带火星的小木条复燃;③ 。
【实验分析】
(1)“小木条复燃”说明Na2O2和CO2反应生成了 ;实验现象③说明该反应放出了热量;同时棉花团是可燃物,棉花团因为同时满足燃烧所需的三个条件,所以燃烧起来了。
(2)请你写出Na2O2和CO2反应的化学方程式
【拓展提高】
同学们在实验室发现一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分及其质量。
【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【猜想与假设】(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是________________________的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物……
【设计实施方案】
| 实验步骤 | 实验现象 |
| ①取15 g变质粉末于一支大试管内,加入适量的水,共收集到1.6g气体,然后用带火星木条检验生成的气体。 | 固体完全溶解,有气泡产生,带火星的小木条复燃 |
| ②继续向上述试管中加入足量的石灰水,充分反应。 | 有白色沉淀生成 |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体5g。 | |
过氧化钠(Na2O2)是一种淡黄色固体。在一次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入了如图1的实验装置中,当倾倒二氧化碳时,发现了 现象;同时也惊奇地发现棉花团燃烧了起来。


【提出问题】棉花团为什么会燃烧起来呢?
【查阅资料】
(1)在常温下Na2O2能和CO2反应生成一种气体和碱性物质。
(2)在常温下Na2O2能和水发生反应: 2Na2O2+2H2O═4NaOH+O2↑
(3)无水硫酸铜为白色固体,吸水后变为蓝色。
【设计实验】经过讨论后,小组同学设计了如图2的实验进行探究。
【实验步骤】
①检查整套装置的气密性;
②把相关的试剂放入对应的仪器内(D装置的U型管内放有足量的Na2O2固体,烧杯内盛有饱和的澄清石灰水),并按图2组装整套实验仪器;
③用力推动针筒的活塞,把稀盐酸注入试管内;
④一段时间后,在P处放置一根带火星的小木条,观察现象。
注:整个实验中不考虑稀盐酸的挥发和空气对实验的影响。

【实验现象】
①无水硫酸铜 ;②带火星的小木条复燃;③ 。
【实验分析】
(1)“小木条复燃”说明Na2O2和CO2反应生成了 ;实验现象③说明该反应放出了热量;同时棉花团是可燃物,棉花团因为同时满足燃烧所需的三个条件,所以燃烧起来了。
(2)请你写出Na2O2和CO2反应的化学方程式
【拓展提高】
同学们在实验室发现一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分及其质量。
【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【猜想与假设】(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是________________________的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物……
【设计实施方案】
|
实验步骤 |
实验现象 |
|
①取15 g变质粉末于一支大试管内,加入适量的水,共收集到1.6g气体,然后用带火星木条检验生成的气体。 |
固体完全溶解,有气泡产生,带火星的小木条复燃 |
|
②继续向上述试管中加入足量的石灰水,充分反应。 |
有白色沉淀生成 |
|
③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体5g。 |
|
【解释与结论】同学们经过认真计算分析,确定了粉末中含有的成分及质量
计算过程:
【反思与评价】
(1)实验室在保存过氧化钠时应注意密封保存。
(2)有同学提出把第②步实验中足量的石灰水改为足量氯化钙溶液,至沉淀不再生成时过滤,向滤液中滴加无色酚酞试液,若液体变红,则证明原粉末中有NaOH。你认为该方案是否合理并说明理由
二氧化硫是形成酸雨的罪魁祸首之一。化学小组的同学想对二氧化硫进行研究,依据化学方程式Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O计算后。取一定量的锌粉与98%的浓硫酸恰好完全反应。
ZnSO4+SO2↑+2H2O计算后。取一定量的锌粉与98%的浓硫酸恰好完全反应。
提出问题:对于制得的气体,有同学认为可能含有杂质。
猜想与假设:化学小组制得的SO2中混有的杂质主要是H2。产生这一结果的主要原因是 (用化学方程式和必要的文字说明)。
查阅资料:(1)CO2能与水、 反应,SO2与CO2一样,也能。
(2)H2与CO一样,能将金属氧化物冶炼成金属。
(3)CaSO3难溶于水
实验验证:为证实相关分析,化学小组的同学设计了下图所示装置进行实验。

(1)B装置的作用是 。
(2)混合气体中含有氢气,则E装置中观察到的现象是 ,反应的化学方程式为 。
实验反思:小芳认为,利用上述装置可以测定混合气体中二氧化硫和氢气的质量比,要达到这一目的,实验小组必须测定下列数据中的 (填字母)。
A.参加反应的锌的质量 B.装置B的质量增量
C.氧化铜的质量 D.装置 F的质量增量
【解析】根据题目给出的信息可知:随着反应的进行,硫酸浓度降低,致使锌与稀硫酸反应生成H2,因此化学小组所制得的气体中混有的主要杂质气体可能是氢气;A是制取气体的装置,B是吸收二氧化硫的装置,可以用氢氧化钠等碱液吸收;C是检验二氧化硫是否除尽的装置,D是浓硫酸,吸水干燥作用;E是用还原性气体还原氧化铜的装置,F中盛放的是无水硫酸铜,检验是否有水生成;G是防止空气中H2O进入干燥管而影响杂质气体的检验.进行解答
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com