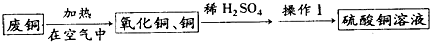(2005?绵阳)(1)硫酸亚铁是一种重要的化工原料,可用作杀虫剂、净水剂和木材防腐剂,还可用来治疗缺铁性贫血.工业上用废铁屑与稀硫酸反应制硫酸亚铁,主要反应的化学方程式为
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
.
废铁屑与硫酸反应产生的气体中含有有毒气体H
2S,用CuSO
4溶液可以吸收这种气体并产生黑色沉淀,该反应的化学方程式为
H2S+CuSO4═CuS↓+H2SO4
H2S+CuSO4═CuS↓+H2SO4
.
(2)为了探究CO的还原性,某同学将绕成螺旋状的铜丝放在酒精灯上加热至铜丝变黑后,立即将铜丝伸入盛满CO的集气瓶中(内装适量澄清石灰水),铜丝又恢复光亮的红色,振荡集气瓶,还可以看到集气瓶中
石灰水变浑浊
石灰水变浑浊
.
上述实验过程中,能表明CO具有还原性的反应的化学方程式是
.将上述表面变黑的铜丝冷却后放入稀硫酸中,可以看到的现象是
黑色固体逐渐消失
黑色固体逐渐消失
溶液由无色变成蓝色
溶液由无色变成蓝色
,
CuO+H2SO4=CuSO4+H2O
CuO+H2SO4=CuSO4+H2O
.
(3)一包白色固体可能含有NaCl、CuSO
4、NH
4NO
3、BaC1
2、K
2 C O
3中的一种或几种.有同学进行下列实验来确定该固体的成分:
(a)取少许固体放入试管,加入NaOH浓溶液并微热,把湿润的红色石蕊试纸放在试管口,试纸变为蓝色.
(b)取一些白色固体放入试管加水溶解,得无色透明溶液.
(c)向实验b所得溶液中滴2滴酚酞试液,溶液变为红色,再向其中加入过量CaC1
2溶液,红色褪去,产生白色沉淀.
(d)将实验c所得溶液中的沉淀滤去,向滤液中加入AgNO
3溶液,又产生白色沉淀.
①根据以上实验现象判断:这包白色固体中一定有
NH4NO3、K2CO3
NH4NO3、K2CO3
,肯定没有
CuSO4、BaC12
CuSO4、BaC12
.
②若用这包白色固体配成稀溶液来浇花,可产生的作用是
AC
AC
(填下列选项的字母序号).
A.促进花草的茎、叶生长茂盛,叶色浓绿
B.促进花草的根系发达,增强抗寒抗旱能力
C.促进花草生长健壮,茎杆粗硬,增强对病虫害和倒伏的抵抗能力
(4)实验室需用20%的稀硫酸(密度为1.14g?cm
-3)460mL,若用如图标签所示的硫酸来配制,则至少需用这种硫酸
58.2
58.2
mL.

 (2005?绵阳)(1)硫酸亚铁是一种重要的化工原料,可用作杀虫剂、净水剂和木材防腐剂,还可用来治疗缺铁性贫血.工业上用废铁屑与稀硫酸反应制硫酸亚铁,主要反应的化学方程式为
(2005?绵阳)(1)硫酸亚铁是一种重要的化工原料,可用作杀虫剂、净水剂和木材防腐剂,还可用来治疗缺铁性贫血.工业上用废铁屑与稀硫酸反应制硫酸亚铁,主要反应的化学方程式为