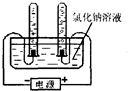
29、小华是个非常爱动脑的同学,做溶液的导电性实验时,小华观察得非常仔细,以下是他们小组观察、记录并思考的一些问题:
(1)电解水时,通常要加入少量氢氧化钠溶液或稀硫酸,目的是
增强溶液的导电性
.
(2)经过溶液的学习后,小华明白了不是所有的溶液都能导电的道理,下列物质加入水中充分振荡后能导电的是
CD
.
A.蔗糖 B.植物油 C.高锰酸钾 D.碳酸钠
(3)做氯化钠溶液的导电性实验时,小华不仅看到灯泡亮了,还观察到与电解水相似的现象:两根石墨电极上都出现了气泡.这激发了小华探究气泡成分的欲望.请你一起参与小华的探究活动吧!
[提出问题]氯化钠溶液通电时石墨电极上分别生成了什么气体?
[查阅资料]Cl
2是黄绿色、有刺激性气味的有毒气体,常温下1体积水能溶解2体积Cl
2.
[提出假设]假设1:电极上分别生成了氢气和氯气;
假设2:电极上分别生成了氧气和氯气;
假设3:电极上分别生成了氢气和氧气.以上假设的依据是
质量守恒定律,化学反应前后,元素种类不变
.
[设计实验]小华决定用右图所示的装置来电解氯化钠的饱和溶液.并收集两个电极上产生的气体.
[实验分析]观察到一支试管中收集的气体为黄绿色,另一支试管中收集到的气体能被点燃,则假设
1
成立:小红又向反应后的溶液中滴加无色酚酞,结果酚酞变红,请写出氯化钠溶液通电时发生反应的化学方程式_
2NaCl+2H2O═2NaOH+H2↑+Cl2↑
.
[反思与评价]联想电解水的实验,你认为在电解水时
不可以
(填“可以”或“不可以”)加入少量的氯化钠溶液,原因是
氯化钠参与反应,影响实验
.
(4)小华还想利用H
2还原氧化铁的实验测定水中氢、氧两种元素的质量比.
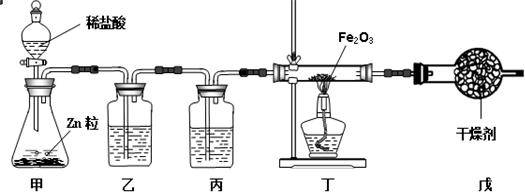
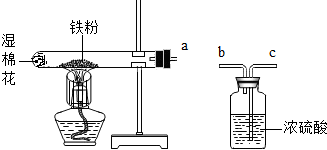
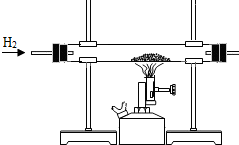
[设计实验]实验装置图如下:
①写出装置中试剂的名称:乙
②氢氧化钠溶液
,丙
浓硫酸
.
②实验开始时,应该先
b
(选填字母).
a.加热反应管丁 b.从分液漏斗中滴加液体
在这两步操作之间,还应进行的一步操作是
检查氢气纯度
.
③写出反应管丁中发生反应的化学方程式:
3H2+Fe2O3═2Fe+3H2O
.
[进行实验]该小组同学进行了实验,测得了下列数据:
|
反应前 |
反应后 |
| 丁管和内盛物的总质量 |
132.4g |
130.0g(冷却到室温称量) |
| 戊管及内盛物的总质量 |
143.2g |
145.9g |
[数据处理]请通过以上数据计算水中氢、氧两种元素的质量比.(请写出计算过程)
mO=2.4g,mH=2.7g-2.4g=0.3g,mH:mO=1:8
[误差分析]
①如果该实验缺少装置丙,则测得的水中氢、氧两种元素的质量比会
偏大
(选填“偏大”或“偏小”).
②如果实验后观察到反应管丁中有水珠凝结,则测得的水中氢、氧两种元素的质量比会
偏大
(选填“偏大”或“偏小”).

 (1)利用高炉尾气中的水蒸气与甲烷催化重整得到合成气,化学方程式为
(1)利用高炉尾气中的水蒸气与甲烷催化重整得到合成气,化学方程式为
 (2013?宁化县质检)宁化县位于福建省西部,总面积2381.3km2,物产丰富.
(2013?宁化县质检)宁化县位于福建省西部,总面积2381.3km2,物产丰富. 29、小华是个非常爱动脑的同学,做溶液的导电性实验时,小华观察得非常仔细,以下是他们小组观察、记录并思考的一些问题:
29、小华是个非常爱动脑的同学,做溶液的导电性实验时,小华观察得非常仔细,以下是他们小组观察、记录并思考的一些问题: