
题目列表(包括答案和解析)
由两种或多种物质混合而成的物质是________,这些物质之间________发生反应,各自________着各自的性质.纯净物由________物质组成,例如________,纯净物有固定的________和确定的________.
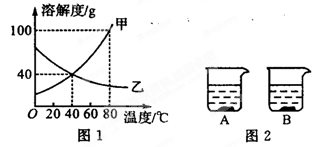
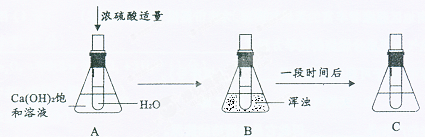
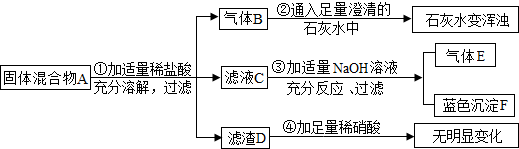
 23、海洋是巨大的资源宝库,从海洋中可提取许多重要物质.请你参与下列探究活动并完成有关问题:
23、海洋是巨大的资源宝库,从海洋中可提取许多重要物质.请你参与下列探究活动并完成有关问题: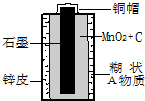 随意丢弃废旧干电池会造成环境污染,而废旧干电池中的许多物质都是可以回收利用的.下面是某化学兴趣小组探究废旧干电池的过程,请帮助他们完成相应的报告:
随意丢弃废旧干电池会造成环境污染,而废旧干电池中的许多物质都是可以回收利用的.下面是某化学兴趣小组探究废旧干电池的过程,请帮助他们完成相应的报告:| 操作步骤 | 实验现象 | 相应的结论 |
| 1.取样.溶于适量的水,静置,过滤.取少量滤液于一支试管中,滴加紫色石蕊试液. | 石蕊试液不变蓝色 | |
| 2.另取少量滤液于另一支试管中,滴加稍过量的稀硝酸. | 无明显现象 | 没有 |
| 3.再向第2步所得溶液中继续滴加少量的 |
没有SO42-存在 | |
| 4.向第3步所得溶液中再滴加少量硝酸银溶液 | 有白色沉淀产生 | 有 |
| 5.取白色糊状物,滴加少量碘溶液 | 有蓝色出现 | 有 |
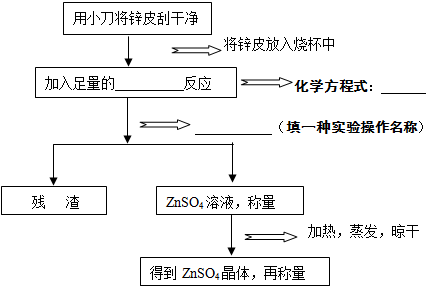
| 废电池1个 | 蒸发皿 | 蒸发皿+ZnSO4溶液 | 蒸发皿+ZnSO4晶体 | |
| 质量/g | 80 | 46.5 | 225.5 | 62.6 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com