
题目列表(包括答案和解析)

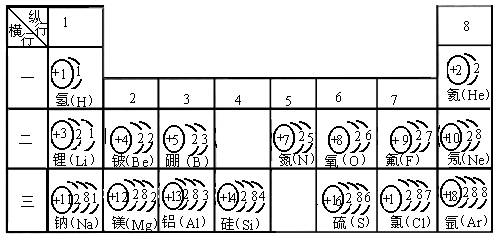
(1)在下列提供的四种元素中,选择相应元素填入上表的空格内(填序号)。
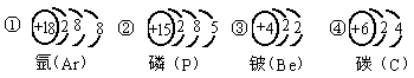
(2)阅读下列短文,回答问题:
实验证明,在上表同一横行中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强;在同一纵行中,从上到下,原子失去电子的能力增强,得到电子的能力减弱。实验还证明,失去电子能力越强的元素,其最高价氧化物的水化物(氢氧化物)的碱性就越强;得到电子能力越强的元素,其最高价氧化物的水化物(含氧酸)的酸性越强,它跟氢气化合形成的氢化物也更稳定。
①在上表元素中,失去电子能力最强的原子是________,得到电子能力最强的原子是________。
②下列判断正确的是________。
A.碱性:Mg(OH)2>Al(OH)3 B.酸性:H2SO4>HClO4(高氯酸)
C.氢化物的稳定性:H2O>H2S D.得到电子能力:Si>N
(3)某元素的原子结构示意图为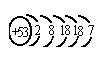 ,则该元素的化学性质跟上表中第________纵行的元素的化学性质最相似。
,则该元素的化学性质跟上表中第________纵行的元素的化学性质最相似。
| 元素名称 | 氢 | 碳 | 氧 | 氯 | 钠 | 铁 |
| 元素符号 | H | C | O | Cl | Na | Fe |
水是人类生活中不可缺少的物质。
(1)下列净水方法中,通常用于除去水中难溶性杂质的是 ,净水程度最高的是 。
| A.过滤 | B.煮沸 | C.蒸馏 | D.吸附 |
水是人类生活中不可缺少的物质。
(1)下列净水方法中,通常用于除去水中难![]() 溶性杂质的是 ① ,净水程度最高的是 ② 。
溶性杂质的是 ① ,净水程度最高的是 ② 。
A.过滤 B.煮沸 C.蒸馏 D.吸附
(2)自来水厂常用二氧化氯(ClO2)消毒,其中氯元素的化合价为__________。
(3)小刚同学设计了电解水简易装置,其中A、B电极由金属曲别针制成。通电后的现象如图所示,则B连电源 ① 极。电解水的化学方程式为 ② 。
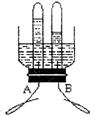
(4)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙(CaCO3)、水和二氧化碳,这就是壶中出现水垢的原因之一。请写出Ca(HCO3)2受热分解的化学方程式__________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com