“碳铵”(NH
4HCO
3)是一种常用的化学肥料,易溶于水,受潮时在常温下就能分解,温度越高分解越快,分解产物为NH
3、CO
2、H
2O.“碳铵”遇碱放出氨气,在土壤中不残留有害物质.
(1)“碳铵”属于化肥中的
肥,化学性质
(填“稳定”或“不稳定”);保存时应
注意
.(选填序号)
①贮存和运输时要密封,不要受潮和曝晒;施用后要立即盖土或立即灌溉
②不要与碱性物质混放或混用
③不能与易燃物质混在一起;结块时,不要用铁锤砸碎
④不宜长期施用
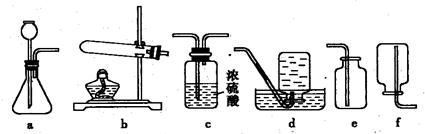
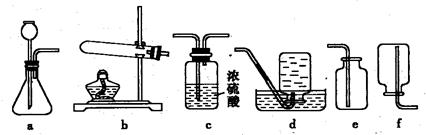
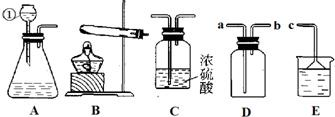
某兴趣小组欲在实验室利用如下图所示的装置研究“碳铵”的部分性质,请你一起参与.
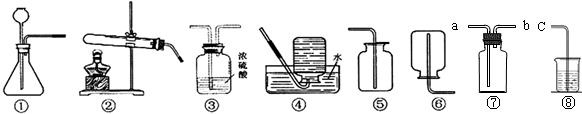
(2)选择装置
(填序号)进行“碳铵”固体受热分解的实验,该反应的化学方程式为
;应用该装置,还可以在实验室进行的实验是
.(答一个即可)
(3)利用装置①,写出实验室制取一种气体的化学方程式
,收集该气体的装置应选择
.
(4)取少量“碳铵”和熟石灰粉末放入装置②的大试管中,微热片刻立即移开酒精灯.将产生的氨气缓缓通入盛有酚酞试液的试管中,酚酞试液变红.
①由此可知,氨气易溶于水,其水溶液(氨水)显
性(填“酸”、“碱”或“中”),pH
7(填“<”、“>”或“=”).
②某同学认为可用装置③干燥氨气你认为他能否达到目的?简要分析原因.
;
③由于氨气具有强烈的刺激性气味,对人体的呼吸道粘膜有较大的伤害,我们可以选用上述的装置中的⑦和⑧连接收集并吸收逸散出来的多余氨气,则应将
(选填“a”或“b”)与c相连接,烧杯中应盛放
.