
题目列表(包括答案和解析)
在1L浓度为c(mol/L)的弱酸HA溶液中,HA、![]() 和
和![]() 的物质的量之和为nc(mol),则HA的电离度为
的物质的量之和为nc(mol),则HA的电离度为
[ ]
在1L浓度为c(mol/L)的弱酸HA溶液中,HA、![]() 和
和![]() 的物质的量之和为nc(mol),则HA的电离度为
的物质的量之和为nc(mol),则HA的电离度为
[ ]
(1)在NaOH溶液中加入一元酸HA溶液,充分反应后,溶液呈中性。甲同学认为溶液中c(Na+)=c(A-),而乙同学认为c(Na+)与c(A-) 是否相等,要看一元酸HA是强酸还是弱酸。你认为 同学的说法正确,理由是 。
(2).已知298K时, MgCO3的Ksp = 6.82×10-6,向1L c(Mg2+ ) = 0.0001 mol·L-1的MgCl2溶液中,滴加Na2CO3浓溶液,假设溶液的体积保持1L不变,当c(CO32-)= 时开始产生沉淀。
(3)已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
在427℃时的平衡常数是9。如果反应开始时,一氧化碳和水蒸气的浓度都是0.001mol/L,则在此反应条件下氧化碳转化率为 。
(16分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)常温下将0.01 mol NH4Cl和0.002 mol NaOH溶于水配成1L溶液。
①溶液中浓度为0.01 mol·L-1的离子是 。
②物质的量之和为0.01 mol的两种粒子是 和 。
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 (填“碱性”、“酸性”或“中性”),醋酸体积 氢氧化钠溶液体积(填“>”、“<”或“=”)。
(3)将m mol·L-1的醋酸和n mol·L-1的氢氧化钠溶液等体积混合后溶液的pH=7, m与n的大小关系是m n。(填“>”、“<”或“=”)
(4)浓度为0.100 mol·L-1的下列各物质的溶液中,c(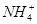 )由大到小的顺序是
)由大到小的顺序是
①NH4Cl ②NH4HSO4 ③NH3·H2O ④CH3COONH4
(5)某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A=H++HA- HA- H++A2-
H++A2-
已知0.1 mol·L-1的NaHA溶液pH=2,则0.1 mol·L-1的H2A溶液中氢离子的物质的量浓度
0.11 mol·L-1(填“>”“=”或“<”)。
(16分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)常温下将0.01 mol NH4Cl和0.002 mol NaOH溶于水配成1L溶液。
①溶液中浓度为0.01 mol·L-1的离子是 。
②物质的量之和为0.01 mol的两种粒子是 和 。
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 (填“碱性”、“酸性”或“中性”) ,醋酸体积 氢氧化钠溶液体积(填“>”、“<”或“=”)。
(3)将m mol·L-1的醋酸和n mol·L-1的氢氧化钠溶液等体积混合后溶液的pH=7, m与n的大小关系是m n。(填“>”、“<”或“=”)
(4)浓度为0.100 mol·L-1的下列各物质的溶液中,c(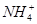 )由大到小的顺序是
)由大到小的顺序是
①NH4Cl ②NH4HSO4 ③NH3·H2O ④CH3COONH4
(5)某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A=H++HA-
HA- H++A2-
H++A2-
已知0.1 mol·L-1的NaHA溶液pH=2,则0.1 mol·L-1的H2A溶液中氢离子的物质的量浓度
0.11 mol·L-1(填“>”“=”或“<”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com