
题目列表(包括答案和解析)
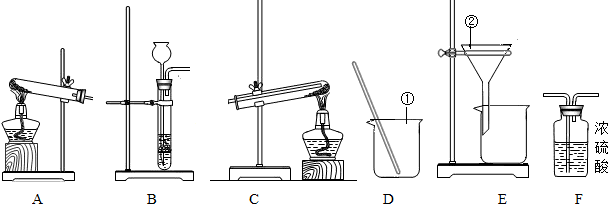
| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是:________ |
| ②将操作①所得的混合物过滤. | 滤液中所含有的溶质是:________ |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜, |

| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是: 使氧化铜完全反应 |
| ②将操作①所得的混合物过滤. | 滤液中所含有的溶质是: CuSO4、H2SO4 |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜, |
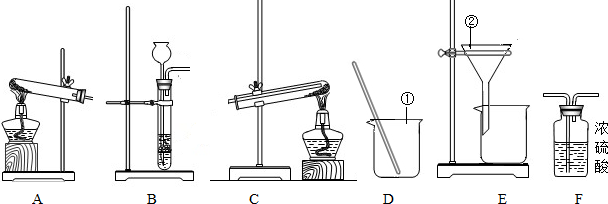
| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是:______ |
| ②将操作①所得的混合物过滤. | 滤液中所含有的溶质是:______ |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜, |
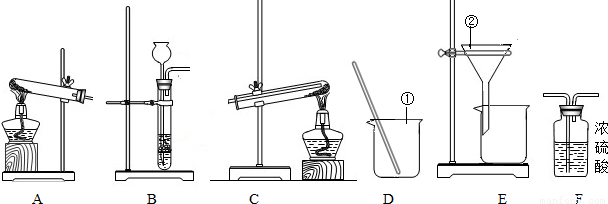
| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是: |
| ②将操作①所得的混合物过滤. | 滤液中所含有的溶质是: |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜, |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com