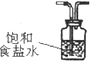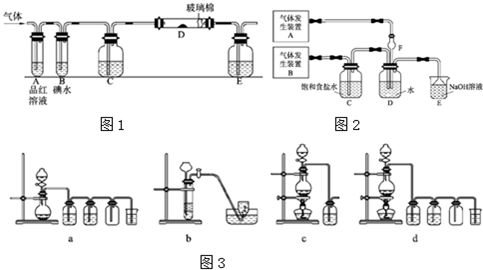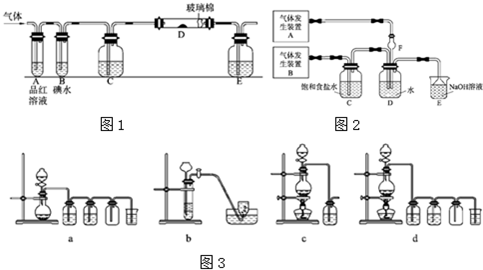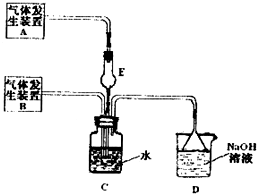
为探究Cl
2、SO
2同时通入H
2O中发生的反应,某化学兴趣小组设计了如右图所示的实验装置.试填空.
(1)请你预测C1
2、SO
2同时通入H
2O中恰好发生反应后的产物(填写离子)
H+、Cl-、SO42-
H+、Cl-、SO42-
.
设计简单的实验验证其中一种阴离子的存在
取反应后的溶液少许于洁净的试管中,滴加氯化钡溶液,若有白色沉淀生成,证明有SO42-存在(或取反应后的溶液少许于洁净的试管中,滴加足量硝酸钡溶液,过滤,在滤液中滴加硝酸银溶液,若有白色沉淀生成证明有Cl-存在).
取反应后的溶液少许于洁净的试管中,滴加氯化钡溶液,若有白色沉淀生成,证明有SO42-存在(或取反应后的溶液少许于洁净的试管中,滴加足量硝酸钡溶液,过滤,在滤液中滴加硝酸银溶液,若有白色沉淀生成证明有Cl-存在).
(2)化学兴趣小组的同学为制取Cl
2,SO
2气体,现采用Na
2SO
3与70%的浓硫酸为原料制取SO
2,采用MnO
2和浓盐酸为原料制取C1
2.在此实验中,E仪器的作用是
防倒吸
防倒吸
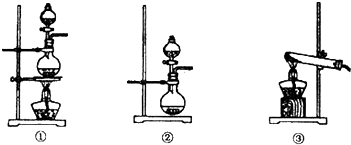
;发生装置B应选择以下三种装置中的
①
①
(填序号).
(3)上述整套装置有一处不合理,应在
B、C
B、C
装置之间(填代号)连接一装置,请在答题纸的方框中画出简易装置图,并注明装置中盛有的试剂
.
(4)下列试剂中的一种就可以验证通入C装置中气体是Cl
2过量还是SO
2过量,该试剂是
④
④
,实验现象及结论为
品红褪色,加热不复原,说明氯气过量;品红褪色,加热又复原,说明二氧化硫过量
品红褪色,加热不复原,说明氯气过量;品红褪色,加热又复原,说明二氧化硫过量
.①氯化钡溶液 ②硝酸银溶液 ③硫氰化钾溶液 ④品红溶液 ⑤液体四氯化碳.

 为探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组设计了如右图所示的实验装置.试填空.
为探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组设计了如右图所示的实验装置.试填空.