
题目列表(包括答案和解析)
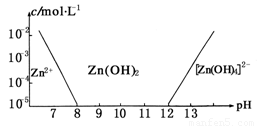
已知锌及其化合物的性质与铝及其化合物相似。如图,横坐标为溶液的pH,纵坐标为Zn2+离子或[Zn(OH)4]2-离子的物质的量浓度(假设Zn2+离子浓度为10-5mol·L-1时,Zn2+离子已沉淀完全)。下列说法不正确的是
A.往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为:
Zn2++4OH-=[Zn(OH)4]2-
B.从图中数据计算可得Zn(OH)2的溶度积Ksp=10-17
C.某废液中含Zn2+离子,沉淀Zn2+离子可以控制溶液pH的范围是8~12
D.向1 L 1 mol·L-1ZnCl2溶液中加入NaOH固体至pH=6,需NaOH 0.2 mol

A.往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为:
Zn2++4OH-![]() [Zn(OH)4]2-
[Zn(OH)4]2-
B.从图中数据计算可得Zn(OH)2的溶度积Ksp=10-17 mol3·L-3
C.某废液中含Zn2+,沉淀Zn2+可以控制溶液pH的范围是8—12
D.向
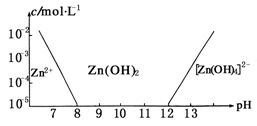
| A.往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为: Zn2++4OH-=[Zn(OH)4]2- |
| B.从图中数据计算可得Zn(OH)2的溶度积Ksp=10-17 |
| C.某废液中含Zn2+离子,沉淀Zn2+离子可以控制溶液pH的范围是8~12 |
| D.向1 L 1 mol·L-1ZnCl2溶液中加入NaOH固体至pH=6,需NaOH 0.2 mol |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com