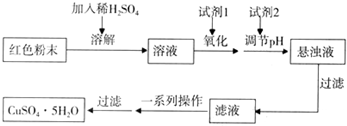
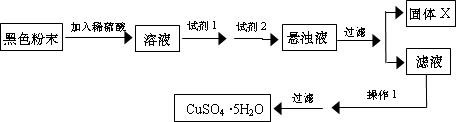
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe
2O
3、Cu
2O或二者混合物.探究过程如下:
查阅资料:Cu
2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO
4,在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe
2O
3 假设2:红色粉末是Cu
2O
假设3:红色粉末是Fe
2O
3和Cu
2O的混合物
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是
没有红色不溶物,滴加KSCN溶液,溶液变为红色
没有红色不溶物,滴加KSCN溶液,溶液变为红色
.
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?
不合理
不合理
,简述你的理由(不需写出反应的方程式 )
Cu能将Fe3+还原为Fe2+
Cu能将Fe3+还原为Fe2+
(3)若固体粉末完全溶解,向所得溶液中滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是
Fe2O3和Cu2O的混合物
Fe2O3和Cu2O的混合物
,写出实验过程中发生的氧化还原反应的离子方程式
Fe2O3+6H+=2Fe3++3H2O、Cu2O+2H+=Cu+Cu2++H2O、2Fe3++Cu=2Fe2++Cu2+
Fe2O3+6H+=2Fe3++3H2O、Cu2O+2H+=Cu+Cu2++H2O、2Fe3++Cu=2Fe2++Cu2+
探究延伸:若经实验分析,确定红色粉末为Fe
2O
3和Cu
2O的混合物.
(4)实验小组欲用加热法测定Cu
2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu
2O的质量分数为
.
(5)某铝土矿样品经测定是由Al
2O
3、Fe
2O
3、FeO、SiO
2等氧化物组成,取样品适量放入烧杯中,加入稀硫酸将其溶解,过滤,取滤液少量于试管中,若证明滤液中含有+2价的铁,选用的试剂和现象为
向滤液加入几滴高锰酸钾溶液,紫红色若能褪去,则说明矿样中含有+2价的铁;反之则没有
向滤液加入几滴高锰酸钾溶液,紫红色若能褪去,则说明矿样中含有+2价的铁;反之则没有
.