
题目列表(包括答案和解析)
某研究性学习小组用如下图装置进行铜与浓硫酸反应的实验研究。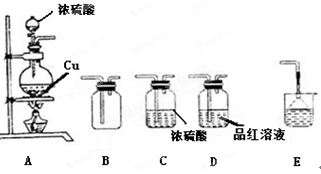
(1)装置A中发生反应的化学方程式 ;
(2)若要使B 中收集满干燥的SO2气体(并证实B中已收集满),则上述装置的连接顺序为: 接 接 接 接 (用字母表示)
(3)待烧瓶中充分反应后,同学们发现铜有剩余。经检测发现硫酸也有剩余.其原因是 ;
检验硫酸有剩余的方法是 .
(4)在不补充浓硫酸的前提下.为使铜进一步溶解,可向烧瓶中加入 (填序号)
①盐酸 ② FeSO4 ③ Fe2O3 ④KNO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com