
题目列表(包括答案和解析)
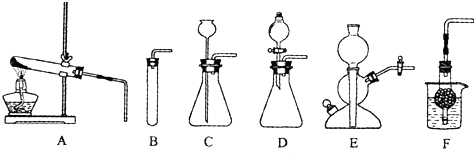
| 比较项目 | 排水法 | 向上排空气法 |
| 收集方法可行性分析 | CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率 | CO2密度比空气大,且______ |
| 收集过程分析 | 集满现象:______ | “验满”分析:因气体无色,故集满与否较难确定.即使用燃着木条移近容器口火焰熄灭,也难以证明空气完全排近 |
| 向收集到CO2的集气瓶内倒入等体积适量澄清石灰水,并振荡 | 先浑浊后变澄清所需时间较短 | 先浑浊后变澄清所需时间较长 |
| 由上述实验可得结论 | (1)______(2)______ | |
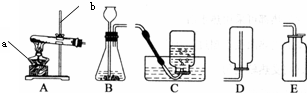
| 药品 | 现象 | 反应速率 | 化学方程式 |
| Na2CO3和稀HCl | 产生大量气泡 | 迅速 | Na2CO3+2HCl=2NaCl+H200+CO2↑ |
| 块状石灰 石和稀HCl | 冒气泡 | 缓和 | ______ |
| 块状石灰 石和稀H2SO4 | 少数几个气泡 | 瞬间即逝 | CaCO3+H2SO4=CaSO4+H2O+CO2↑ |
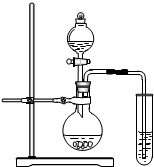 下列是初三某合作学习小组实验室制取二氧化碳气体的研究过程,请你参与其中.
下列是初三某合作学习小组实验室制取二氧化碳气体的研究过程,请你参与其中.| 比较项目 | 排水法 | 向上排空气法 |
| 收集方法可行性分析 | CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率 | CO2密度比空气大,且 不与空气反应 不与空气反应 . |
| 收集过程分析 | 集满现象: 集气瓶口有气泡冒出 集气瓶口有气泡冒出 . |
“验满”分析:因气体无色,故集满与否较难确定.即便用燃着木条移近容器口火焰熄灭,也难以证明空气完全排尽. |
| 向收集到的CO2集气瓶内倒入等体积适量澄清石灰水,并振荡 | 先浑浊后变澄清所需时间较短. | 先浑浊后变澄清所需时间较长. |
| 由上述实验可得结论 | ① 二氧化碳可用排水法或向上排空气法收集 二氧化碳可用排水法或向上排空气法收集 ;②用排水法收集到的二氧化碳比较纯净 用排水法收集到的二氧化碳比较纯净 . | |
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积(mL) | 35 | 47 | 55 | 51 | 42 |
| 试管编号 | A | B | C | D | E |
| 温度(℃) | 40 | 50 | 60 | 70 | 80 |
| 现象和 比较 |
有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温用盐酸反应相似 | 反应激烈,迅速产生大量气体 |
 下列是初三某合作学习小组实验室制取二氧化碳气体
下列是初三某合作学习小组实验室制取二氧化碳气体| 比较项目 | 排水法 | 向上排空气法 |
| 收集方法可行性分析 | CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率 | CO2密度比空气大, 不与空气发生反应 不与空气发生反应 . |
| 收集过程分析 | 集满现象: 集气瓶口有气泡冒出 集气瓶口有气泡冒出 . |
“验满”分析:因气体无色,故集满与否较难确定.即便用燃着木条移近容器口火焰熄灭,也难以证明空气完全排尽. |
| 向收集到的CO2集气瓶内倒入等体积适量澄清石灰水,并振荡 | 先浑浊后变澄清所需时间较短. | 先浑浊后变澄清所需时间较长. |
| 由上述实验可得结论 | ① 二氧化碳可用排水法或向上排空气法收集; 二氧化碳可用排水法或向上排空气法收集; ;②用排水法收集到的二氧化碳比较纯净 用排水法收集到的二氧化碳比较纯净 . | |
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积(mL) | 35 | 47 | 55 | 51 | 42 |
| 试管编号 | A | B | C | D | E |
| 温度(℃) | 40 | 50 | 60 | 70 | 80 |
| 现象和 比较 |
有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温用盐酸反应相似 | 反应激烈,迅速产生大量气体 |
| 比较项目 | 排水法 | 向上排空气法 |
| 收集方法可行性分析 | CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率 | CO2密度比空气大,且 . |
| 收集过程分析 | 集满现象: . | “验满”分析:因气体无色,故集满与否较难确定.即便用燃着木条移近容器口火焰熄灭,也难以证明空气完全排尽. |
| 向收集到的CO2集气瓶内倒入等体积适量澄清石灰水,并振荡 | 先浑浊后变澄清所需时间较短. | 先浑浊后变澄清所需时间较长. |
| 由上述实验可得结论 | ① ;② . | |
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积(mL) | 35 | 47 | 55 | 51 | 42 |
| 试管编号 | A | B | C | D | E |
| 温度(℃) | 40 | 50 | 60 | 70 | 80 |
| 现象和 比较 | 有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温用盐酸反应相似 | 反应激烈,迅速产生大量气体 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com