
题目列表(包括答案和解析)


 所示,则该元素的原子序数为
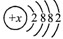
所示,则该元素的原子序数为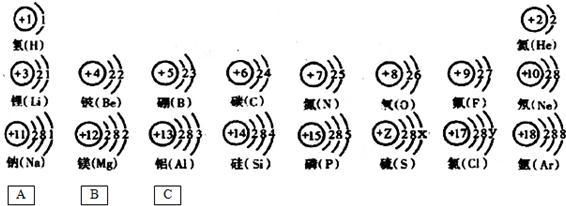
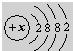 该元素在上表中位于
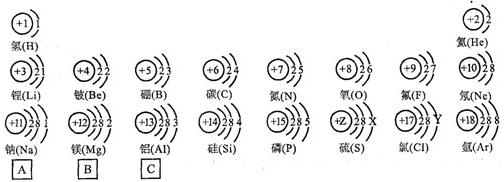
该元素在上表中位于 氢(H) 氢(H) |  氦(He) 氦(He) | ||||||
 锂( Li) 锂( Li) |  铍(Be) 铍(Be) |  硼(B) 硼(B) |  碳(C) 碳(C) | 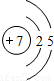 氮(N) 氮(N) |  氧(O) 氧(O) |  氟(F) 氟(F) |  氖(Ne) 氖(Ne) |
 钠(Na) 钠(Na) |  镁(Mg) 镁(Mg) |  铝(Al) 铝(Al) |  硅(Si) 硅(Si) |  磷(P) 磷(P) |  硫(S) 硫(S) |  氯(Cl) 氯(Cl) | 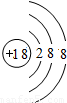 氩(Ar) 氩(Ar) |
| A | B | C | |||||
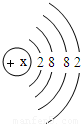 元素在上表中位于______(选A、B、C)处.
元素在上表中位于______(选A、B、C)处.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com