
题目列表(包括答案和解析)
| 氢氧化钠 体积:500mL 化学式:NaOH 相对分子质量:40 密度:1.5 g/cm3 质量分数:50%(1)用20mL氢氧化钠溶液可以配制质量分数为10%的氢氧化钠溶液 (2)利用刚配制好的氢氧化钠除去混有RCl2的NaCl固体(R代表某二价金属).取20g该固体样品,全部溶解在100g水中,再加入刚配制好的溶液80g,混合到恰好完全反应后过滤,得到固体的质量为9.8g. ①题中发生反应的化学方程式为 ②利用已知条件求解反应生成NaCl质量(x)的比例式为 ③R的元素符号是 ④原混合物中NaCl的质量分数为 ⑤向反应后所得溶液中加入173.8g水,则此时溶液中溶质的质量分数是 实验室有一瓶氢氧化钠浓溶液,瓶上标签内容如图所示,请你根据标签上提供的数据解答下列问题:
(2)利用刚配制好的氢氧化钠除去混有RCl2的NaCl固体(R代表某二价金属).取20g该固体样品,全部溶解在100g水中,再加入刚配制好的溶液80g,混合到恰好完全反应后过滤,得到固体的质量为9.8g. ①题中发生反应的化学方程式为______; ②利用已知条件求解反应生成NaCl质量(x)的比例式为______; ③R的元素符号是______; ④原混合物中NaCl的质量分数为______; ⑤向反应后所得溶液中加入173.8g水,则此时溶液中溶质的质量分数是______. 27、实验室里有一瓶标签残缺的盐酸,请你参与下列有关问题的研讨. (1)怎样立即确定该瓶盐酸是浓盐酸?有人猜测是,有人记得好象不是,大家各抒已见,你认为,应该用下列中的 C 方法;(填编号)A、讨论 B、调查 C、实验 D、上网 具体做法是 打开瓶盖,观察瓶口上方是否有白雾出现 .(2)某同学想粗略测定该盐酸每亳升中含溶质HCl的质量,他依据酸和碱中和反应的原理,设计了一种实验方案,其操作步骤如下: 第一步,在小烧杯中加入10g5%的NaOH溶液; 第二步,向上述烧杯中滴入2滴酚酞试液; 第三步,向10mL的量筒里注入该盐酸至一定刻度; 条四步,用胶头滴管吸取量筒中的盐酸,逐滴滴入上述烧杯中,滴到溶液由红色刚刚变为无色为止,将胶头滴管中的剩余液体全部滴入量筒中; 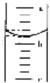 第五步,记录实验数据; 第六步,计算确定每毫升盐酸中含溶质HCl的质量. 请根据以上实验过程,回答下列问题: ①本实验为什么要用指示剂(酚酞)?答: 用指示剂可以确定盐酸滴加到什么时候氢氧化钠与盐酸恰好完全反应. ;②第三步中向量筒注入盐酸,量筒中液面的位置如图所示,a与b、b与c刻度间均相差1mL,如果刻度a为4,量筒中盐酸的体积是 3.2ml ;③第四步要用到玻璃棒,它的用途是 搅拌 ,目的是让盐酸和氢氧化钠充分接触,使其反应完全. ;④第五步要记录的数据是 量筒中剩余盐酸的量 ;(3)实验结束后有的同学认为,在(2)中测定每毫升盐酸中含溶质HCl的质量的原理和方法还有多种.请你利用所学的化学知识再写出几种其他方案(用文字简述所依据的原理和要测定的数据,不需要写化学方程式). 方法一: 称量一个小烧杯的质量,向该烧杯中加入一定量的盐酸,再加入一定量的过量的锌粒,待无气泡冒出后,称量装置的总质量.反 应前后装置减少的质量为氢气的质量,根据氢气的质量可求出所加盐酸中溶质的质量 ;方法二: 向烧杯中加入一定量的的盐酸,再加入一定量的过量的氧化铜,待充分反应后,过滤、洗涤、干燥并称量剩余氧化铜的质量,根 据参加反应的氧化铜的质量可求出所加盐酸中溶质的质量 ;方法三: 称量一个小烧杯的质量,向该烧杯中加入一定量的盐酸,再加入一定量的过量的大理石,待无气泡冒出后,称量装置的总质量. 反应前后装置减少的质量为二氧化碳的质量,根据二氧化碳的质量可求出所加盐酸中溶质的质量 .某中学化学实验室有如图所示的实验装置,用于制取氧气、二氧化碳等多种气体.  (1)请写出有标号仪器的名称:① 试管 试管 ②酒精灯 酒精灯 (2)若制取的一种气体是 氧气 氧气 ,应选用的收集装置是C或D C或D (填序号,下同),应选用的发生装置是A A ,反应的化学方程式是2KMnO4
2KMnO4 ;检验所制取的气体的方法是:
将带火星的木条伸入集气瓶内,若木条复燃则是氧气 将带火星的木条伸入集气瓶内,若木条复燃则是氧气 ;(3)在常温下,用亚硫酸钠固体和稀硫酸制取二氧化硫气体,应选用的发生装置是: B B ;由于二氧化硫是易溶于水、密度比空气大的有毒气体,所以应用E E 装置进行收集,以便将尾气吸收处理,避免造成大气污染 大气污染 (4)该中学化学课外兴趣小组同学利用发生装置B进行“石块中是否含有碳酸钙”的探究活动.在活动中小明发现,相邻小组气体产生的速率比自己小组的快.小明将这一情况报告老师,老师鼓励他们对此问题共同探究. 【提出问题】影响二氧化碳气体产生速率的因素是什么? 【作出猜想】①不同地点石块中碳酸钙含量不同; ②所用的盐酸不同; ③还可能是 石块的大小不同(或石块质量不同、盐酸质量不同) 石块的大小不同(或石块质量不同、盐酸质量不同) .【设计实验】(1)验证猜想①是否成立,要设计的实验:分别取大小相同、质量相同、 不同地点 不同地点 的石块,加入相同的稀盐酸进行实验.【交流讨论】实验中可以通过观察 放出气泡的剧烈程度不同 放出气泡的剧烈程度不同 ,粗略地比较反应速率.【拓展延伸】上述实验中,小明采用了控制单一变量的研究方法.用此方法探究“催化剂对用过氧化氢溶液制取氧气的反应速率的影响”,需要控制不变的因素有 过氧化氢溶液的浓度、温度(合理均可) 过氧化氢溶液的浓度、温度(合理均可) 等(答出一点即可). (7分)如下图所示为实验室中常见气体制备、净化、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。某学校 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |