
题目列表(包括答案和解析)
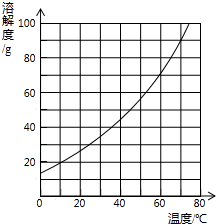 如图是固体A的溶解度曲线示意图,下表是固体B在不同温度时的溶解度.
如图是固体A的溶解度曲线示意图,下表是固体B在不同温度时的溶解度.| 温度/℃ | O | 20 | 40 | 60 | 80 |
| 溶解度/g | 32 | 35 | 40 | 50 | 65 |
 (已知硝酸钾、硝酸钠、碳酸锂不同温度时的溶解度(见下表)
(已知硝酸钾、硝酸钠、碳酸锂不同温度时的溶解度(见下表)溶解度/g 温度 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 |
| 硝酸钠 | 69.5 | 82.3 | 100.6 | 121.8 | 148.4 |
| 碳酸锂 | 1.55 | 1.33 | 1.18 | 1.00 | 0.82 |
溶解度/g 温度/℃ 物质 | 0 | 20 | 40 | 60 | 80 | 100 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
(1)若采用加入溶质的方法使溶液成为饱和溶液,则应加入硝酸钾晶体多少克?
(2)若以蒸发溶剂的方法使溶液成为饱和溶液,则应蒸发掉多少克水?
(3)若以降低温度的方法使溶液成为饱和溶液,则应降到多少度时溶液才能达到饱和状态?
温度/℃ 0 10 15 20 26 30
溶解度/g 13.3 20.9 25 31.6 40 45.8
| 温度/℃ | 20 | 40 | 60 | 80 |
| 溶解度/g | 40 | 50 | 58 | 68 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com