
题目列表(包括答案和解析)
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
| 元素 | 相关信息 |
| A | A元素原子核外只有三个能级,且每个能级上含有相等的电子数 |
| B | 是客气中含量最丰富的元素 |
| C | 短周期元素中,C的金属性最强 |
| D | 基态原子第三能层上有7种运动状态不同的电子 |
| E | 一种核素的质量数为63,中子数为34 |

下图中A、B均为固体,其中B为单质.下图可用于工业生产F,F是衡量一个国家化工水平的标志.回答下列问题:
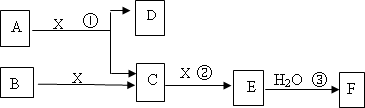
(1)A的化学式________
(2)反应①是一个氧化还原反应,该反应发生时,每生成4 mol气体C,转移电子________mol
(3)写出D与铝单质反应的化学方程式________
(4)反应②是可逆反应,在2 L的密闭容器中投入4 mol C和3 mol X,10分钟后反应达到平衡,平衡时混合气体共6 mol,则下列说法正确的是________
A.工业制取F时,C和X生成E的反应是在吸收塔进行
B.这10分钟内,X的平均速率是0.1 mol/(L·min)
C.当C和X的消耗速率比为2∶1时,标志着反应达到平衡
D.平衡时C的转化率是50%
E.在工业生产中可以通过增加X的量来提高C的转化率
F.工业生产中直接用水来吸收E
(5)写出2.24 L气体C与0.15 mol氢氧化钠溶液反应的离子化学方程式________
(6)将5 mL 0.02 mol/L的F溶液与5 mL 0.02 mol/L NaOH溶液充分混合,若混合后溶液的体积为10 mL,则混合液的pH是________写出F的一种用途________
(每空3分,共15分)已知四种元素A、B、C、D,其原子序数依次增大,最外层电子依次为4、1、2、7,其中A元素原子次外层电子数为2,B、C 两元素的原子次外层电子数为8,B元素原子最外层电子数比第1层电子数少1,也比C元素原子第M层电子数少1,D元素的单质为液态非金属单质。若此四种元素均位于元素周期表前四个周期,按要求填写下列各题:
⑴ A元素的气态氢化物用电子式表示为_______________________________,
D元素在周期表中的位置为_____________________________________。
⑵ B元素的最高价氧化物的水化物用电子式表示为
⑶ C、D两元素形成的化合物属于__________化合物,用电子式表示其生成过程为
_____________________________________________________________________。
(每空3分,共15分)已知四种元素A、B、C、D,其原子序数依次增大,最外层电子依次为4、1、2、7,其中A元素原子次外层电子数为2,B、C 两元素的原子次外层电子数为8,B元素原子最外层电子数比第1层电子数少1,也比C元素原子第M层电子数少1,D元素的单质为液态非金属单质。若此四种元素均位于元素周期表前四个周期,按要求填写下列各题:
⑴ A元素的气态氢化物用电子式表示为_______________________________,
D元素在周期表中的位置为_____________________________________。
⑵ B元素的最高价氧化物的水化物用电子式表示为
⑶ C、D两元素形成的化合物属于__________化合物,用电子式表示其生成过程为
_____________________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com