23ЎўЈЁ1Ј©ЛбЎўјоЎўСОИЬҪвРФұнКЗС§П°»ҜС§өДЦШТӘ№ӨҫЯЈ®УТұнБРіцБЛЎ°Іҝ·ЦЛбЎўјоЎўСОФЪ20ЎжКұөДИЬҪвРФЎұЈ®Зл°ҙПВБРТӘЗуМоРҙУР№ШДЪИЭЈә
ІйИЬҪвРФЈәCuЈЁOHЈ©
2І»ИЬ
Ј®
Рҙ»ҜС§КҪЈәТ»ЦЦ»У·ўРФЛб
HCl
Ј®
ЕР¶ПЈәNaNO
3УлBaCl
2ИЬТәДЬ·с·ўЙъ·ҙУҰЈҝ
І»ДЬ
ЈЁМоЎ°КЗЎұ»тЎ°·сЎұЈ©Ј»АнУЙКЗ
І»·ыәПёҙ·ЦҪв·ҙУҰөДМхјю
Ј»
РҙіцМъ»тВБУлұнЦРөДТ»ЦЦСО·ҙУҰөД»ҜС§·ҪіМКҪЈә
Fe+CuSO4=FeSO4+Cu
ЈЁ2Ј©ЙъІъ№в»¬ЦҪХЕК№УГөДЎ°ұө°ЧЎұУРТ»ЦЦЦЖ·ЁЈ¬ўЩУГСОЛбҙҰАнМјЛбұөЈ»ўЪПтЛщөГИЬТәјУИлБтЛбЈ®РҙіцЎ°ұө°ЧЎұөДЦчТӘіЙ·ЦөД»ҜС§КҪЈә
BaSO4
Ј»Рҙіц·ҙУҰўЪөД»ҜС§·ҪіМКҪЈә
BaCl2+H2SO4ЁTBaSO4Ўэ+2HCl
ЈЁ3Ј©ўЩЕЁБтЛбәНПЎБтЛбЈ¬ФЪКөСйКТЦРіЁҝЪ·ЕЦГЈ¬ЛьГЗөДЦКБҝәН·ЕЦГМмКэөД№ШПөИзУТПВНјЈ®
aЎўbЗъПЯЦРұнКҫЕЁБтЛбөДКЗЈЁМоЧЦДёРтәЕЈ©
b
Ј»АнУЙКЗ
ЕЁБтЛбОьКХҝХЖшЦРөДЛ®·Ц¶шК№ЦКБҝФцҙу
Ј®
ўЪПВНјКЗБҪЦЦПЎКНЕЁБтЛбөДІЩЧчЈә
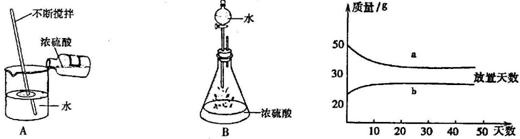
ЙПГжБҪНјЦРЈ¬ПЎКНЕЁБтЛбІЩЧчХэИ·өДКЗЈЁМоРтәЕЈ©
A
Ј¬AНјЦРІЈБ§°фөДЧчУГКЗ
ҪБ°и
Ј®BНјЦРІЈБ§өј№ЬөДЧчУГКЗ
ЙўИИ
Ј®
ЈЁ4Ј©ўЩДіКҜ»Ҝі§УРТ»ЦЦКҜУНІъЖ·ә¬УРЦКБҝ·ЦКэОӘ4.9%өДІРУаБтЛбЈ¬№эИҘЛыГЗ¶јКЗУГNaOHИЬТәАҙЗеПҙХвР©БтЛбЈ®ИфТӘЗеПҙ100kgөДХвЦЦКҜУНІъЖ·Ј¬АнВЫЙПРиТӘNaOH
4
kgЈ®
ўЪКҜ»Ҝі§ҪшРРБЛјјКхёДФмЈ¬ёДУГCaЈЁOHЈ©
2ЦРәНХвР©ІРУаБтЛбЈ®ГҝҙҰАн100kgХвЦЦІъЖ·Ј¬ҝЙТФҪЪФј¶аЙЩҫӯ·СЈҝ
NaOHәНCaЈЁOHЈ©
2өДКРіЎјЫёсИзПВұнЈә
| ГыіЖ |
NaOH |
CaЈЁOHЈ©2 |
| јЫёсЈЁФӘ/kgЈ© |
24.00 |
6.00 |


 18ЎўЙХұӯЦРКўУРxИЬТәЈ¬ЦрөОјУИлЈЁ»тНЁИлЈ©yОпЦКЈ¬ЙХұӯДЪТәМеөДpHұд»ҜИзНјЛщКҫЈ®Фт·ыәПёГұд»ҜөДТ»ЧйОпЦККЗЈЁЎЎЎЎЈ©
18ЎўЙХұӯЦРКўУРxИЬТәЈ¬ЦрөОјУИлЈЁ»тНЁИлЈ©yОпЦКЈ¬ЙХұӯДЪТәМеөДpHұд»ҜИзНјЛщКҫЈ®Фт·ыәПёГұд»ҜөДТ»ЧйОпЦККЗЈЁЎЎЎЎЈ©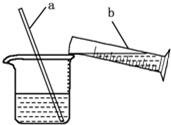 25ЎўПВНјКЗПЎКНЕЁБтЛбКөСйөДКҫТвНјЈ®
25ЎўПВНјКЗПЎКНЕЁБтЛбКөСйөДКҫТвНјЈ®