
题目列表(包括答案和解析)



(13分)化学是一门以实验为基础的学科,通过一年的学习,相信你的实验能力一定有了很大提高,请你一同参与回答以下问题。
(一)某实验小组设计了下图所示的实验装置。
⑴ 写出仪器A的名称
⑵ 甲同学认为打开K1、关闭K2时,利用I、Ⅱ装置,可以制取并收集氧气,该化学反应方程式为 : 。
⑶乙同学认为利用Ⅰ、Ⅲ装置可以测定空气中氧气的含量。关闭K、K1、K2,用凸透镜引燃B中的白磷,待冷却后打开K2,整个实验过程中能观察到的现象是:① ;② 。
⑷ 丙同学认为可以利用Ⅰ、Ⅲ装置验证二氧化碳能与氢氧化钠溶液发生反应。他在广口瓶B中预先收集满二氧化碳气体,在仪器A中盛放氢氧化钠浓溶液,烧杯中盛放稀盐酸, K1关闭、K2打开,然后打开K将氢氧化钠浓溶液滴入广口瓶中,关闭K,依据 现象,可以证明二氧化碳能与氢氧化钠溶液发生化学反应。
(二)甲、乙两同学对有关镁与盐酸的反应进行了系列研究(如图)
探究一:镁与盐酸反应过程中的能量变化以及反应速率的变化:`
⑴实验时需将镁条进行打磨,其目的是 。
⑵反应中试管外壁发烫,说明镁与稀盐酸反应是放热反应,化学方程式为 。
⑶实验测得镁片产生气体的速率(v)与时间(t)的关系如图所示,你认为在t1~t2时间内反应速率逐渐加快的主要原因是: 。
探究二:.反应后所得溶液的酸碱性探究
【发现问题】
⑴反应后甲同学用pH试纸测定试管中溶液的酸碱性,发现pH小于7,说明甲同学所得溶液呈 性,(选填“酸”“碱”或“中”)。
⑵反应后乙同学的试管中镁条有剩余,向试液中滴入两滴酚酞溶液,溶液变红。
【查阅资料】氢氧化镁微溶于热水,且溶解度随温度升高而增大。
【提出猜想】
甲同学:猜想Ⅰ:稀盐酸过量,使溶液pH小于7;
猜想Ⅱ:氯化镁溶液pH小于7。
乙同学:猜想Ⅰ:氯化镁溶液呈碱性使酚酞变成红色;
猜想Ⅱ:镁与热水反应后生成碱使酚酞变红色。
【实验与思考】
⑴为验证猜想,甲、乙两同学均需测定____溶液的酸碱性,实验表明该溶液显弱酸性。
⑵乙同学为验证猜想Ⅱ,在滴有两滴酚酞的热水中放入一段打磨过的镁条,观察到溶液很快变为红色,同时还观察到镁条表面有气泡产生,收集并点燃该气体,发现气体能燃烧,请根据以上现象写出镁与热水反应的化学方程式 ;
⑶乙同学在进行上述猜想Ⅱ的探究时,发现实验一段时间后,酚酞的红色总是会逐渐消失,于是他猜想可能是镁与热水反应后生成的碱逐渐被空气中的二氧化碳反应掉了,但甲同学猜想可能是水温逐渐降低,导致 ,请你设计一个简单的实验方案验证甲或乙的猜想是否成立 (写出相应的操作、现象和结论): 。
【结论】
镁与稀盐酸反应,若镁反应完全后所得溶液显酸性,若镁过量时所得溶液显碱性。
(13分)化学是一门以实验为基础的学科,通过一年的学习,相信你的实验能力一定有了很大提高,请你一同参与回答以下问题。
(一)某实验小组设计了下图所示的实验装置。
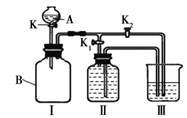
⑴ 写出仪器A的名称
⑵ 甲同学认为打开K1、关闭K2时,利用I、Ⅱ装置,可以制取并收集氧气,该化学反应方程式为 : 。
⑶乙同学认为利用Ⅰ、Ⅲ装置可以测定空气中氧气的含量。关闭K、K1、K2,用凸透镜引燃B中的白磷,待冷却后打开K2,整个实验过程中能观察到的现象是:① ;② 。
⑷ 丙同学认为可以利用Ⅰ、Ⅲ装置验证二氧化碳能与氢氧化钠溶液发生反应。他在广口瓶B中预先收集满二氧化碳气体,在仪器A中盛放氢氧化钠浓溶液,烧杯中盛放稀盐酸, K1关闭、K2打开,然后打开K将氢氧化钠浓溶液滴入广口瓶中,关闭K, 依据 现象,可以证明二氧化碳能与氢氧化钠溶液发生化学反应。
(二)甲、乙两同学对有关镁与盐酸的反应进行了系列研究(如图)

探究一:镁与盐酸反应过程中的能量变化以及反应速率的变化:`
⑴实验时需将镁条进行打磨,其目的是 。
⑵反应中试管外壁发烫,说明镁与稀盐酸反应是放热反应,化学方程式为 。
⑶实验测得镁片产生气体的速率(v)与时间(t)的关系如图所示,你认为在t1~t2时间内反应速率逐渐加快的主要原因是: 。

探究二:.反应后所得溶液的酸碱性探究
【发现问题】
⑴反应后甲同学用pH试纸测定试管中溶液的酸碱性,发现pH小于7,说明甲同学所得溶液呈 性,(选填“酸”“碱”或“中”)。
⑵反应后乙同学的试管中镁条有剩余,向试液中滴入两滴酚酞溶液,溶液变红。
【查阅资料】氢氧化镁微溶于热水,且溶解度随温度升高而增大。
【提出猜想】
甲同学:猜想Ⅰ:稀盐酸过量,使溶液pH小于7;
猜想Ⅱ:氯化镁溶液pH小于7。
乙同学:猜想Ⅰ:氯化镁溶液呈碱性使酚酞变成红色;
猜想Ⅱ:镁与热水反应后生成碱使酚酞变红色。
【实验与思考】
⑴为验证猜想,甲、乙两同学均需测定____溶液的酸碱性,实验表明该溶液显弱酸性。
⑵乙同学为验证猜想Ⅱ,在滴有两滴酚酞的热水中放入一段打磨过的镁条,观察到溶液很快变为红色,同时还观察到镁条表面有气泡产生,收集并点燃该气体,发现气体能燃烧,请根据以上现象写出镁与热水反应的化学方程式 ;
⑶乙同学在进行上述猜想Ⅱ的探究时,发现实验一段时间后,酚酞的红色总是会逐渐消失,于是他猜想可能是镁与热水反应后生成的碱逐渐被空气中的二氧化碳反应掉了,但甲同学猜想可能是水温逐渐降低,导致 ,请你设计一个简单的实验方案验证甲或乙的猜想是否成立 (写出相应的操作、现象和结论): 。
【结论】
镁与稀盐酸反应,若镁反应完全后所得溶液显酸性,若镁过量时所得溶液显碱性。
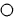 表示氧原子、
表示氧原子、 表示碳原子,反应的方程式为__________________________两种反应的化学计量系数(用符号表示)为____________________该示意图说明了化学反应的实质是___________________________
表示碳原子,反应的方程式为__________________________两种反应的化学计量系数(用符号表示)为____________________该示意图说明了化学反应的实质是___________________________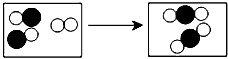
目前全球正面临着能源、环境、水资源、粮食等方面的危机。
(1)目前人类通过化学反应获得的能量大多来自化石燃料。福州市民陆续使用天然气,写出天然气在空气中完全燃烧的化学反应方程式:_____________________________________。化石燃料的使用,给人们的生活带来很多的方便,同时也对环境造成了不良影响。如:煤燃烧时会排放出二氧化硫(SO2)、二氧化氮(NO2)等污染物, 煤燃烧同时提高了空气中的二氧化碳的浓度,会引起 。低碳生活是指生活中要尽量减少能量消耗和材料消耗,从而降低二氧化碳的排放量。下列做法符合低碳生活理念的是 。(填字母序号) A.少用一次性的木筷 B.用完电器后拔掉插头C.大力发展火力发电 D.优化建筑设计,研制新型保温材料 (2)“水是生命之源”,饮用酸碱度过大或硬度过大的水都不利于人体健康。检验水是硬水还是软水,可用的物质是 。请你说出生活中使硬水软化的一种常用方法 。 (3)随着水资源的减少,粮食产量将会受到严重影响。粮食中的主要成分为淀粉,淀粉属于 (填“蛋白质”“维生素”“油脂”或“糖类”),是人体能量的主要来源。 (4)从2011年5月1日起,驾驶员酒醉后驾车要负刑事责任。让司机向酒精检测仪吹气,通过显示的颜色变化,可测出司机是否酒后驾车。其化学反应原理如下: C2H5OH+ 4X(红棕色)+ 6H2SO4 ="2" Cr2 (SO4)3(绿色) + 2CO2↑+ 9H2O,则X的化学式为 (5)菠萝适宜生长在pH为5~6的土壤环境中,在菠萝生长过程中,为了防治病虫害,可适时喷洒农药波尔多液(熟石灰和硫酸铜的混合液)。成熟的菠萝果实香甜可口。根据上述材料回答下列问题: A.菠萝适宜生长在 (填“酸性”、“碱性”或“中性”)的土壤里;
B.从事菠萝种植的果农们在配制农药波尔多液时,均使用塑料桶或木桶,而不使用铁桶,其原因是(用化学方程式表示): ; C.采果收成后结合防治病虫害,可施加些磷酸二氢钾作根外追肥。磷酸二氢钾属于_____ (填“氮肥”、“磷肥”、“钾肥”或“复合肥”) (6)汽车是现代生活中不可缺少的代步工具。请回答下列问题: A、下列汽车配件及用品中,用合金制做的是(填字母) 。a.钢铁外壳 b.玻璃车窗 c.橡胶轮胎 d.真皮座椅B、铁在潮湿的空气中容易锈蚀。汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝空气(氧气)和__________。C、尾气催化转化器”可将汽车尾气中的有毒气体转化为无毒气体,下图表示治理汽车尾气所涉及反应的微观过程。  图中所示反应的化学方程式为 ;
图中所示反应的化学方程式为 ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com