
题目列表(包括答案和解析)
向密闭的容器中通入氧气(含a个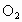 分子)和一氧化氮(含b个NO分子)气体,已知:
分子)和一氧化氮(含b个NO分子)气体,已知: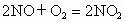 ,则最终容器内氧原子和氮原子个数之比为
,则最终容器内氧原子和氮原子个数之比为
[
]|
A .2(a+b)/b |
B .2a/b |
|
C .(2a+b)/b |
D .b/a |
向密闭的容器中通入氧气(含a个 分子)和一氧化氮(含b个NO分子)气体,已知:
分子)和一氧化氮(含b个NO分子)气体,已知: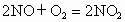 ,则最终容器内氧原子和氮原子个数之比为
,则最终容器内氧原子和氮原子个数之比为
[
]|
A .2(a+b)/b |
B .2a/b |
|
C .(2a+b)/b |
D .b/a |
向密闭的容器中通入氧气(含a个氧气分子)和一氧化氮(含有b个一氧化氮分子)气体,已知:2NO+O2====2NO2,则最终容器内氧原子和氮原子个数之比为( )
A.2(a+b)/b B.2a/b C.(2a+b)/b D.b/a
向密闭的容器中通入氧气(含a个氧气分子)和一氧化氮(含有b个一氧化氮分子)气体,已知:2NO+O2====2NO2,则最终容器内氧原子和氮原子个数之比为( )
A.2(a+b)/b B.2a/b C.(2a+b)/b D.b/a
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com