
题目列表(包括答案和解析)
 (2012?广陵区二模)珍珠粉由珍珠经加工制成的白色粉末,是重要的药品、化妆品原料.市场上出现的假珍珠粉外观上与真珍珠粉差不多,肉眼无法辨别它们.但假珍珠使用过多会带来健康问题.
(2012?广陵区二模)珍珠粉由珍珠经加工制成的白色粉末,是重要的药品、化妆品原料.市场上出现的假珍珠粉外观上与真珍珠粉差不多,肉眼无法辨别它们.但假珍珠使用过多会带来健康问题.| 操作 | 现象 | 结论与化学反应方程式 |
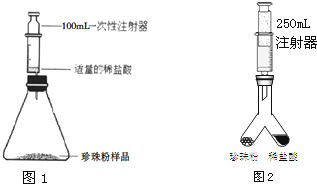
分别取真假珍珠粉个稍许置于两只试管中,加一定量的稀盐酸后迅速塞紧橡皮塞,将导管的另一端放入石灰水中,观察 |
试管a中均有气泡产生 试管b中实验现象 石灰水变浑浊 石灰水变浑浊 ; |
都含有碳酸盐 a中的化学反应方程式 CaCO3+2HCl═CaCl2+CO2↑+H2O CaCO3+2HCl═CaCl2+CO2↑+H2O ,b中化学反应方程式 Ca(OH)2+CO2═CaCO3↓+H2O Ca(OH)2+CO2═CaCO3↓+H2O ; |
分别取真假珍珠粉稍许置于两只试管c、d中,滴加一定量的浓硝酸,静置后观察 |
C试管内部 有 有 (填“有”、“没有”)少量黄色固体出现;d试管中 没有 没有 (填“有”、“没有”)气泡,无黄色固体出现. |
真珍珠粉中含有少量的蛋白 质 假珍珠粉中不含蛋白质 |
| 样品种类 | 第一次 | 第二次 | 第三次 |
| 假珍珠粉样品(ml) | 110.50 | 110.28 | 110.05 |
| 真珍珠粉样品(ml) | 103.82 | 103.16 | 102.82 |
| 序号 | 实验内容 | 实验现象 | 实验结论 |
| ① | 取少量样品于烧杯中,滴加稀盐酸 | 有大量气泡生成 | 本格不填 |
| ② | 用铂丝蘸取①中溶液,在酒精灯上灼烧 | 火焰为砖红色 | 溶液中含有钙离子 |
| ③ | 另取少量样品于烧杯中,加水充分溶解,滴加 碘水或碘酒 碘水或碘酒 |
无蓝色出现 | 样品中不含有淀粉 |
| ④ | 另取少量样品于烧杯中,加水溶解,静置、过滤,在滤液中加入适量浓硝酸,加热至沸 | 产生黄色固体 产生黄色固体 |
样品中含蛋白粉 (氨基酸) |
| 100 |
| x |
| 44 |
| 0.44g |
| 1g |
| 1.1g |
| 100 |
| x |
| 44 |
| 0.44g |
| 1g |
| 1.1g |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com