
题目列表(包括答案和解析)
二、有机化学反应式:
5、![]()
6、CH2 =CH2 + Br2![]() CH2BrCH2Br
CH2BrCH2Br
7、CH2 =CH2 + H2O ![]() CH3CH2OH
CH3CH2OH
8、
![]()
9、![]()
11、CH ≡ CH + Br2![]() CHBr=CHBr
CHBr=CHBr
CHBr = CHBr+ Br2![]() CHBr2CHBr2
CHBr2CHBr2
12、
![]()

14、
![]()
15、
![]()
16、
![]()
17、

18、![]()
19、

20、2CH3CH2OH+2Na![]() 2CH3CH2ONa+ H2↑ü
2CH3CH2ONa+ H2↑ü
21、
![]()
23、![]()
25、![]()
26、

27、
28、
29、CH3CHO +2Ag(NH3)2OH ![]() H2O+2Ag↓?+3NH3+CH3COONH4
H2O+2Ag↓?+3NH3+CH3COONH4
30、乙醛与新制氢氧化铜悬浊液反应:Cu2+ +2OH- = Cu(OH)2↓?
![]()
31、2CH3COOH+Na2CO3![]() 2CH3COONa+CO2↑ +H2O
2CH3COONa+CO2↑ +H2O
32、
33、CH3COOCH2CH3+H2O![]() CH3COOH +CH3CH2OH
CH3COOH +CH3CH2OH
35、![]()
一、有机物的官能团:
3、卤(氟、氯、溴、碘)原子:-X 4、(醇、酚)羟基:-OH
5、醛基:-CHO 6、羧基:-COOH
二、有机反应类型:
取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。
加成反应:有机物分子里不饱和的碳原子跟其他原子或原子团直接结合的反应。
加成聚合(加聚)反应:不饱和的单体聚合成高分子的反应。
消去反应:从一个分子脱去一个小分子(如水.卤化氢),因而生成不饱和化合物的反应。 氧化反应:有机物得氧或去氢的反应。 还原反应:有机物加氢或去氧的反应。
酯化反应:醇和酸起作用生成酯和水的反应。
水解反应:化合物和水反应生成两种或多种物质的反应(有卤代烃、酯、糖等)
同分异构体:几种化合物具有相同的分子式,但具有不同的结构式。 1、碳架异构2、官能团位置异构3、官能团种类异构(即物质种类改变了):醇/酚、羧酸/酯、烯醇/醛 三、有机物燃烧通式烃:CxHy+(x+![]() )O2 → xCO2+
)O2 → xCO2+![]() H2O 烃的含氧衍生物: CxHyOz+(x+
H2O 烃的含氧衍生物: CxHyOz+(x+![]() -
-![]() )O2 → xCO2+
)O2 → xCO2+![]() H2O
H2O
四、有机合成路线:

补充:
1、
、各类有机物的通式、及主要化学性质 烷烃CnH2n+2 仅含C—C键 与卤素等发生取代反应、热分解 烯烃CnH2n 含C==C键 与卤素等发生加成反应、与高锰酸钾发生氧化反应、聚合反应 炔烃CnH2n-2 含C≡C键 与卤素等发生加成反应、与高锰酸钾发生氧化反应、聚合反应 苯(芳香烃)CnH2n-6 与卤素等发生取代反应、与氢气等发生加成反应 (甲苯、乙苯等苯的同系物可以与高锰酸钾发生氧化反应) 卤代烃:CnH2n+1X 醇:CnH2n+1OH或CnH2n+2O 苯酚:遇到FeCl3溶液显紫色 醛:CnH2nO 羧酸:CnH2nO2 酯:CnH2nO2 蛋白质:浓的无机盐(NH4)2SO4.Na2SO4使其盐析;加热.紫外线.X射线.强酸.强碱.重金属(Pb2+.Cu2+.Hg2+)及
有机物(甲醛.酒精.苯甲酸)使蛋白质变性;浓硝酸使蛋白质颜色变黄;蛋白质灼烧时,会有焦味.
五、有机物燃烧通式烃:CxHy+(x+![]() )O2 → xCO2+
)O2 → xCO2+![]() H2O 烃的含氧衍生物: CxHyOz+(x+
H2O 烃的含氧衍生物: CxHyOz+(x+![]() -
-![]() )O2 → xCO2+
)O2 → xCO2+![]() H2O
H2O
六、有机合成路线:

补充:
1、

2、

3、

4、
![]()
5、

6、

7、

8、
![]()
9、
 10、
10、

11、

12、

13、
![]()
14、
![]()
15、

16、
![]()
锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱.但是氢氧化铝不溶于氨水而氢氧化锌能溶于氨水生成[Zn(NH3)4]2+.回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为________(用化学式表示);
(2)写出锌跟氢氧化钠溶液反应的离子方程式______________________;
(3)下列各组中的两种溶液,用相互滴加的方法即可鉴别的是________
①硫酸铝和氢氧化钠
②硫酸铝和氨水
③硫酸锌和氨水
④偏铝酸钠和盐酸
⑤碳酸氢钠和氢氧化钙
锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水而氢氧化锌能溶于氨水生成[Zn(NH3)4]2+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为 (用化学式表示);
(2)写出锌跟氢氧化钠溶液反应的离子方程式 ;
(3)下列各组中的两种溶液,用相互滴加的方法即可鉴别的是
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氨水 ④偏铝酸钠和盐酸 ⑤碳酸氢钠和氢氧化钙
非金属知识规律总结
【高考导航】
一、非金属元素在周期表中的位置和结构特点
1、除H外,非金属元素均在“阶梯线”的右上方。共有16种非金属元素,其中包括稀有气体元素6种。
2、非金属元素(包括稀有元素)均在主族(零族)。非金属元素一般都有变价。
3、最外层电子数一般≥4(H、B除外)。
4、原子半径比同周期金属半径小(稀有元素除外)。
二、非金属性强弱的判断依据
元素非金属性的本质是元素的原子吸引电子的能力。试题常通过以下几个方面来比较元素的非金属性:
1、单质跟H2化合难易程度(反应条件,剧烈程度,反应热的大小,生成气态氢化物的稳定性)。
2、最高价氧化物对应水化物的酸性。
3、化合物中元素化合价的正负,如BrCl中,Cl为-1价,Br为+1价,说明非金属性Cl>Br。
4、通过氧化还原反应确定非金属单质的氧化能力,进而比较非金属性。
需要指出的是,非金属单质的活动性与非金属元素的活动性,有密切的联系,但不是一回事。例如氮元素的非金属性相当强,可是它的单质N2化学性质却不很活泼。单质的化学性质不仅取决于原子结构,而且取决于分子结构和晶体结构。
三、非金属元素的性质及递变规律
1、单质:
(1)结构:除稀有气体外,非金属原子间以共价键结合。非金属单质的成键有明显的规律性。若它处在第N族,每个原子可提供8-N个价电子去和8-N个同种原子形成8-N个共价单键,可简称8-N规则;(H遵循2-N规则)。如ⅦA族单质:x-x;H的共价数为1,H-H,第ⅥA族的S、Se、Te共价单键数为8-6=2,第ⅤA族的P、As共价单键数8-5=3。但第二周期的非金属单质中N2、O2形成多键。
(2)熔沸点与聚集态。它们可以分为三类:
①小分子物质。如:H2、O2、N2、Cl2等,通常为气体,固体为分子晶体。
②多原子分子物质。如P4、S8、As4等,通常为液态或固态。均为分子晶体,但熔、沸点因范德华力较大而比①高,Br2、I2也属此类,一般易挥发或升华。
③原子晶体类单质。如金刚石、晶体硅和硼等,是非金属单质中高熔点“三角区”,通常为难挥发的固体。
(3)导电性:非金属一般属于非导体,金属是良导体,而锗、硅、砷、硒等属于半导体。但半导体与导体不同之处是导电率随温度升高而增大。
(4)化学活性及反应:

③非金属一般为成酸元素,难以与稀酸反应。 固体非金属能被氧化性酸氧化。

2、氢化物:
(1)气态氢化物性质比较
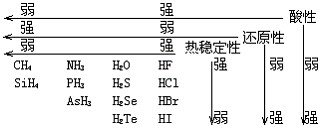
(2)由于氢键的存在,使得第ⅤA、ⅥA、ⅦA氢化物的熔沸点出现了反常。第ⅤA中:SbH3>NH3>AsH3>PH3;第ⅥA中: H2O>H2Te>H2Se>H2S;第ⅦA中HF>HI>HBr>HCl。
(3)气态氢化物水溶液的酸碱性及与水作用的情况。①HCl、HBr、HI溶于水成酸且都是强酸。②HF、H2S、H2Se、H2Te溶于水成酸且都是弱酸。③NH3溶于水成碱,氨水是弱碱。④PH3、AsH3、CH4与水不反应。⑤SiH4、B2H6与水作用时分解并放出H2。
3、非金属氧化物的通性:
(1)许多非金属低价氧化物有毒,如SO2、NO、NO2、CO等,注意不能随便排放于大气中。
(2)非金属氧化物(除SiO2外)大都是分子晶体,熔沸点相差不大。
(3)非金属氧化物大都为酸酐,相应的酸易溶于水,则氧化物易与水化合,反之水化反应难以进行。
(4)不成盐氧化物(如CO、NO)不溶于水,也不与碱反应。虽然NO2能与碱反应生成盐,但NO2不属于酸酐。
4、含氧酸
(1)同周期非金属元素最高价含氧酸从左到右酸性增强。
(2)氧化性:同种元素低价强于高价含氧酸.
如:HClO>HClO3>HClO4(稀)
H2SO3>H2SO4(稀)
HNO2>HNO3(稀)
(3)对于同种非金属形成的不同含氧酸,价态越高,酸性越强。其顺序如:HClO4>HClO3>HClO2>HClO,H2SO4>H2SO3。
(4)难挥发的H2SO4、H3PO4受热难分解;强氧化性的HNO3、HNO2、HClO见光或受热易分解;非氧化性的H2CO3、H2SO3易分解。强酸可制弱酸,难挥发性酸制挥发性酸。
(5)常见含氧酸的一般性质:
①H2SO4:无色粘稠的油状液体,强酸,沸点高,不挥发,稳定。浓硫酸有吸水性、脱水性和强氧化性。
②H2SO3:仅存在于溶液中,中强酸,不稳定。
③HClO4:在水溶液中相当稳定,最强无机酸,有强氧化性。
④HClO:仅存在于溶液中,是一种弱酸,有强氧化性和漂白性,极不稳定,遇光分解。⑤HNO3:无色液体,强酸,沸点低,易挥发,不稳定,易分解,有强氧化性。
⑥H3PO4:无色晶体,中强酸,难挥发,有吸水性,稳定,属于非氧化性酸。
⑦H2CO3:仅存在于溶液中,弱酸,不稳定。
⑧H2SiO3:白色固体,不溶于水,弱酸,不挥发,加热时可分解。
⑨常见酸的酸性强弱。强酸:HCl、HNO3、H2SO4;中强酸:H2SO3>H3PO4(H3PO4中强偏弱);弱酸:HF>CH3COOH>H2CO3>H2S>HClO>H2SiO3。
四、11种无机化学气体的制取和性质(O2、H2、Cl2、CO、NO、SO2、NO2、CO2、H2S、HCl、NH3)。
(1)利用氧化还原反应原理制取的气体有:O2、H2、Cl2、NO、NO2等。
(2)利用复分解制取的气体有:SO2、CO2、H2S、HCl、NH3等。
(3)可用启普发生器制取的气体有:H2、CO2、H2S等。
(4)只能用排气法收集的是:Cl2、SO2、NO2、CO2、H2S、HCl、NH3等。只能用排水法收集的气体是:NO、CO。
(5)使红色石蕊变蓝的气体是NH3;使石灰水变浑浊的气体是SO2和CO2;使品红溶液褪色的气体是SO2和Cl2;使高锰酸钾溶液和溴水褪色的气体有H2S和SO2。
(6)臭鸡蛋气味的气体是H2S;刺激性气味的气体有:Cl2、SO2、NO2、HCl、NH3等;毒性气体有:Cl2、CO、NO、SO2、NO2、H2S等。
(7)能在空气中燃烧的气体:H2S、CO、H2等
已知A、B、C、D、E为原子序数递增的五种短周期元素,A与C、B与D同主族。请回答:
(1)C2B2的电子式 ,A2B2属于 晶体(“分子”、“原子”或“离子”)。
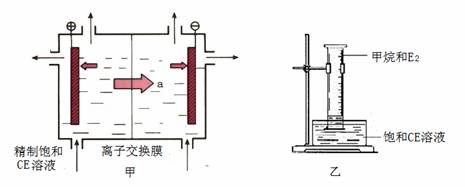
(2)甲装置是离子交换膜法电解饱和CE溶液的原理示意图。透过交换膜的离子a是___,电解的离子方程式 。
(3)为检验E2的性质,某同学做了如下实验:
①Cu丝在E2中燃烧的现象 ,你认为Fe丝在E2也可点燃的理由是 。
a.Fe与Cu都是金属元素
b.Fe的熔点比Cu高
c.Fe的密度比Cu小
d.Fe的金属性比Cu强
②将乙装置放置在光亮的地方(日光没有直接照射),一段时间后,观察到量筒壁上有油状液滴生成,量筒内气体颜色变浅等。生成的物质有 种,水槽中的液体用饱和CE溶液而不用水的原因是 。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
(4)D的单质能跟C的最高价氧化物对应的水化物的浓溶液发生氧化还原反应,生成的两种正盐的水溶液均呈碱性写出该氧化还原反应的离子方程式![]() 。
。
(5)用铂作电极电解1L含有0.4molCuDB4和0.2molCE的水溶液,一段时间后在一个电极上得到了0.3molCu,在另一极上析出的气体在标况下的体积是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com