某学生设计如图甲实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
(1)A仪器的名称是______,D的作用______.
(2)漂白粉将在U型管中产生,其化学反应方程式是______.
(3)有同学建议在两个橡皮套管内的玻璃管口应尽量紧靠,原因是______
(4)此实验结果所得Ca(ClO)
2产率太低.经分析并查阅资料发现主要原因是在U型管中存在两个副反应:1度较高时氯气与消石灰反应生成了Ca(ClO
3)
2,为避免此副反应的发生,可采取的措施是______,有同学测出了反应后溶液中ClO
-、ClO
3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为如图乙(不考虑氯气和水的反应).
a、图中曲线I表示______离子的物质的量随反应时间变化的关系.
b、所取石灰乳中含有Ca(OH)
2的物质的量为______mol.
c、另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl
-的物质的量为0.37mol,则产物中n(ClO
-)/n(ClO
3-)=______
②试判断另一个副反应是(写出此反应方程式)______;为避免此副反应发生,可采取的措施是______
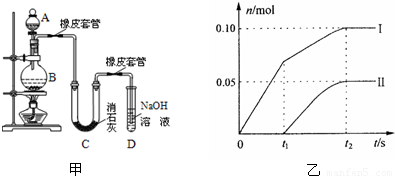

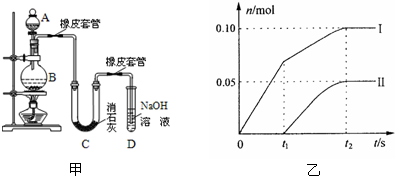


 某学生设计如图所示实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应,反应后温度将升高),A中盛浓盐酸,C中盛潮湿的消石灰,据此回答下列问题:
某学生设计如图所示实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应,反应后温度将升高),A中盛浓盐酸,C中盛潮湿的消石灰,据此回答下列问题: