
题目列表(包括答案和解析)
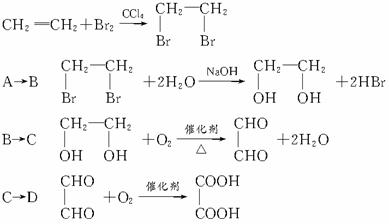
图1-4-20
请完成下列各题:
(1)写出结构简式:A_________,F_________,C_________。
(2)反应类型:X_________、Y_________。
(3)写出化学反应方程式:
A→B____________________________________;
G→H____________________________________。
(4)若环状酯E在NaOH溶液中共热,则发生反应的化学方程式为__________________。
| 实验步骤 | 预期现象和结论 |
| ①取铜与浓硫酸反应所得的绿色溶液于试管中,多次震荡,静置 ②取铜与稀硝酸反应所得的蓝色溶液通NO2气体 ③ |
溶液颜色由绿色转变为深蓝色,证明假设二成立 蓝色溶液变成绿色,证明假设二成立 |

现有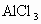 和
和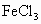 混合溶液,其中
混合溶液,其中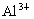 和
和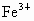 的物质的量之和为0.1mol,在此溶液中入
的物质的量之和为0.1mol,在此溶液中入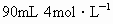 的NaOH溶液,使其充分反应.设
的NaOH溶液,使其充分反应.设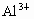 物质的量与总物质的量的比值x.
物质的量与总物质的量的比值x.
(1)根据反应的化学方程式计算x=0.4时,溶液中产生的沉淀是什么?物质量有多少?
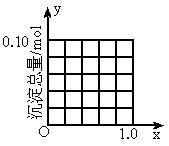
(2)计算沉淀中只有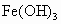 时x的取值范围.请在上图中画出淀总量
时x的取值范围.请在上图中画出淀总量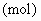 随
随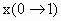 变化的曲线
变化的曲线
(3)若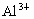 和
和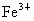 的物质的量之和为
的物质的量之和为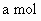 (a为合理数值).其他条件不变时,求沉淀中同时有
(a为合理数值).其他条件不变时,求沉淀中同时有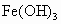 、
、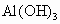 的x的取值范围和各沉淀的物质的量(用含有a、x的式子表示).
的x的取值范围和各沉淀的物质的量(用含有a、x的式子表示).
已知硝酸锏溶液颜色为蓝色
.某学校化学课外小组同学们在做铜与浓硝酸、稀硝酸反应的实验中,发现铜和浓硝酸反应后溶液为绿色旦有红棕色气体产生,而铜和稀硝酸反应后溶液为蓝色,产生无色气体.为弄清反应后溶液颜色出现差异的原因,他们进行了实验探究.实验:在两支试管中各放入一小块
等质量的铜片,分别加人等体积的浓HNO3(14 mol·L-1)和稀HNO3(4 mol·L-1),立即用蘸有NaOH的棉花封住试管口.充分反应后铜均无剩余.(1)Cu与浓HNO3反应的离子方程式________
(2)用蘸有NaOH的棉花封住试管口的原因________
已知NO2与NaOH溶液反应中,其中NO2的还原产物是亚硝酸盐(NO![]() )
)
写出反应的化学反应式________,
提出假设:假设一、因为铜离子浓度大造成的.
假设二、溶液呈绿色是因为铜与浓硝酸反应时产生的二氧化氮溶于过量浓硝酸,加上和蓝色的硝酸铜溶液混在一起,使溶液呈绿色.
设计实验方案,验证假设:
(3)上述实验________(“能”或“不能”)证明假设一不成立,原因________
(4)甲同学设计实验验证假设二,请帮他完成下表中内容(提示:NO![]() 在不同条件下的还原产物较复杂,有时难以观察到气体产生)
在不同条件下的还原产物较复杂,有时难以观察到气体产生)

分析推理:
(5)铜和稀硝酸反应后溶液为蓝色的原理________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com