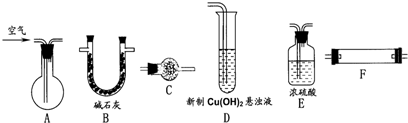
( I)某无色稀溶液X中,可能含有下表所列离子中的某几种.
| 阴离子 |
CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 |
Al3+、Cu2+、Mg2+、NH4+、Na+ |
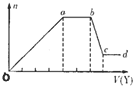
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂Y体积(V)的关系如图所示.
(1)若Y是盐酸,则溶液中含有的金属阳离子是
,ab段发生反应的总离子方程式为
,Oa段上表中参加反应的离子的物质的量之比为:
[要标明离子符号,如n(Na
+)].
(2)若Y是NaOH溶液,则bc段反应的离子方程式为
.若不考虑离子的水解因素,忽略H
+和OH
-影响,且溶液中只存在四种离子,则它们的离子个数比为
[按阳离子在前,阴离子在后,高价在前,低价在后的顺序排列].
( II)锡为第IVA族元素,锡的单质和化合物与某些物质的化学性质上有许多相似之处.已知锡元素具有如下性质:①Sn
4++Sn═2Sn
2+;②2Sn
2++O
2+4H
+═2Sn
4++2H
2O;③2H
++SnO
22-?Sn(OH)
2?Sn
2++2OH
-,试回答:
(1)锡溶于盐酸,再向反应后的溶液中通入氯气,有关反应类似于铁的相应变化,试写出有关反应的化学方程式:
,
.
(2)将(1)中溶液蒸干后继续加热所得固体,变化过程类似于FeCl
3溶液相应的变化,则最后得到的固体物质是(分子式)
.
(3)若可用SnCl
2溶液与过量的碱溶液反应的方法制Sn(OH)
2,该碱是
.

 ( I)某无色稀溶液X中,可能含有下表所列离子中的某几种.
( I)某无色稀溶液X中,可能含有下表所列离子中的某几种. 某无色稀溶液X中,可能含有下表所列离子中的某几种.
某无色稀溶液X中,可能含有下表所列离子中的某几种.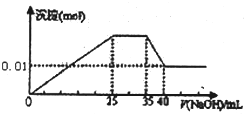 有一未知的无色溶液,只可能含有以下离子中的若干种:H+、NH+4、K+、Mg2+、Cu2+、Al3+、NO-3、CO2-3、SO2-4,现取三份100mL溶液进行如下实验
有一未知的无色溶液,只可能含有以下离子中的若干种:H+、NH+4、K+、Mg2+、Cu2+、Al3+、NO-3、CO2-3、SO2-4,现取三份100mL溶液进行如下实验