
题目列表(包括答案和解析)
| 7m1 |
| 30 |
| 7m1 |
| 30 |
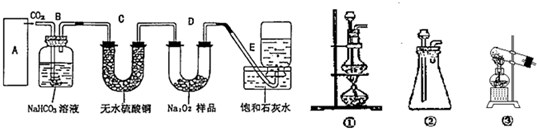


Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如图所示装置进行有关实验。
(1)实验前,装置的气密性检验方法是 。
(2)该装置中,碱石灰的作用是 ;实验开始时,先打开a、b产生氢气,一段时间后,再点燃酒精灯加热,目的是 。
(3)在启普发生器中,下列做法可以加快生成氢气速率的有 。
A.滴加少量的硫酸铜溶液 B.铁粒改用相同量的铁粉 C.稀盐酸改为浓度为其2倍的稀硝酸 D.适当加热
(4)若实验过程中观察到淡黄色粉末变成白色,干燥管内硫酸铜变成蓝色。则Na2O2与H2反应的化学方程式为 。
(5)实际实验过程中观察到Na2O2熔化后,很快变成白色粉末,但干燥管内硫酸铜并未变成蓝色。则Na2O2与H2反应的化学方程式为 。
(6)出于实验安全考虑,实验结束时 。
A.应先关闭活塞b,然后移去酒精灯
B.应先移去酒精灯,然后关闭活塞b
C.A和B都可以
Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如图所示装置进行有关实验。
(1)实验前,装置的气密性检验方法是 。
(2)该装置中,碱石灰的作用是 ;实验开始时,先打开a、b产生氢气,一段时间后,再点燃酒精灯加热,目的是 。
(3)在启普发生器中,下列做法可以加快生成氢气速率的有 。
A.滴加少量的硫酸铜溶液 B.铁粒改用相同量的铁粉 C.稀盐酸改为浓度为其2倍的稀硝酸 D.适当加热
(4)若实验过程中观察到淡黄色粉末变成白色,干燥管内硫酸铜变成蓝色。则Na2O2与H2反应的化学方程式为 。
(5)实际实验过程中观察到Na2O2熔化后,很快变成白色粉末,但干燥管内硫酸铜并未变成蓝色。则Na2O2与H2反应的化学方程式为 。
(6)出于实验安全考虑,实验结束时 。
A.应先关闭活塞b,然后移去酒精灯
B.应先移去酒精灯,然后关闭活塞b
C.A和B都可以
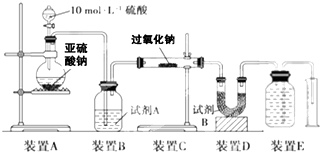
过氧化钠(Na2O2)是中学常见物质,常见的过氧化物还包括过氧化钙(CaO2)。已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成。有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。
实验一:向一定量的过氧化钠固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。
(1)提出假设:
假设1:反应后固体中只有Na2SO3,证明SO2未被氧化;
假设2:反应后固体中只有Na2SO4,证明SO2完全被氧化;
假设3:__________________________证明______________________。
实验探究:
实验二:通过测量气体的体积判断发生的化学反应,实验装置如下:

(2)试剂A可以选用________,试剂B的作用是________。
(3)实验测得装置C中过氧化钠质量增加了m1 g,装置D质量增加了m2 g,装置E中收集到的气体为V L(已换算成标准状况下),用上述有关测量数据判断,SO2未被氧化、完全被氧化的V-m1关系式。
未被氧化:____________,完全被氧化:____________。
(4)若SO2完全被氧化,写出反应的化学方程式: __________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com