
题目列表(包括答案和解析)
在给定条件下,下列加点的物质在对应的化学反应中能完全耗尽的是
A.向100.0 mL 5.00 mol/L的稀硝酸中加入5.6 g铁
B.用40.0 mI,10.00 mol/L的盐酸与10.0 g二氧化锰共热制取氯气
C.标准状况下,将1.0 g铝片投入20.0 mL,18.40 mol/L的硫酸中
D.在一定条件下,用5 mol氧气和1 mol二氧化硫合成三氧化硫
| A、中性溶液的pD=7.0 | B、含0.01 mol的NaOD的D2O溶液1 L,其pD=12.0 | C、溶解0.01 mol DCl的D2O溶液1 L,其pD=2.0 | D、在100 mL 0.25 mol?L-1的DCl重水溶液中,加入50 mL 0.2 mol?L-1的NaOD的重水溶液,其pD=1.0 |
| 组分 | HCOOR | H2O | HCOOH } | ROH |
| 物质的量浓度/mol?L-1’ | 1.00 | 1.99 | 0.01 | 0.52 |
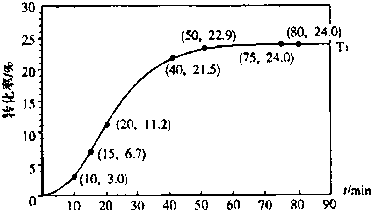
| 反应时间/min | 0~5 | 10~15 | 20~25 | 30~35 | 40~45 | 50~55 | 75~80 |
| 平均速率/10-3mol?L-1?min-1 | 1.9 | 7.4 | 7.8 | 4.4 | 1.6 | 0.8 | 0.0 |
| c(ROH)c(HCOOH) |
| c(HCOOR)c(H2O) |
| c(ROH)c(HCOOH) |
| c(HCOOR)c(H2O) |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com